题目内容
将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是
A.CO2 B.NH3 C.NO2 D.H2S
A
【解析】
试题分析:由于酸性HCl>H2SO3; 所以将SO2通入BaCl2溶液至饱和,未见沉淀生成;A、若通入CO2气体,溶液仍然呈酸性,而且酸性H2SO3>H2CO3.所以不能发生反应,没有任何现象发生,正确;B、若通入NH3,则形成氨水,会与H2SO3反应产生(NH4)2SO3, SO32-+Ba2+=BaSO3↓,产生白色沉淀,错误;C、若通入NO2,该气体与水发生产生硝酸,硝酸有强氧化性,会把H2SO3氧化为H2SO4。H2SO4与BaCl2形成BaSO4白色沉淀,错误;D、若通入H2S,则会发生反应:2H2S+ SO2=3S↓+2H2O,形成淡黄色沉淀,错误。
考点:考查SO2、与其它气体通入BaCl2溶液中发生反应的现象的知识。

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
下列数据是对应物质的熔点
Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
920 | 801 | 1291 | 190 | -107 | 2073 | -57 | 1723 |
据此做出的下列判断中错误的是
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
 NaAlO2(aq)
NaAlO2(aq)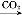 Al(OH)3 ②S
Al(OH)3 ②S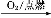 SO3
SO3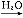 H2SO4
H2SO4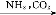 NaHCO3
NaHCO3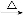 Na2CO3
Na2CO3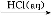 FeCl3(aq)
FeCl3(aq) Mg(OH)2
Mg(OH)2 MgO
MgO