题目内容
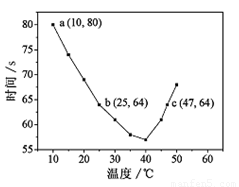
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020mol·L-1NaHSO3(含少量淀粉)10.0ml、KIO3(过量)酸性溶液40.0ml混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是

- A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
- B.图中b、c两点对应的NaHSO3反应速率相等
- C.图中a点对应的NaHSO3反应速率为5.0 ×10-5mol·L-1·s-1
- D.温度高于40℃时,淀粉不宜用作该试验的指示剂
B
A、从图像中可以看出,40℃以前,温度越高,反应速度越快,40℃后温度越高,变色时间越长,反应越慢,而55℃,未变蓝,说明没有生成I2,正确;B、b、c点对应的反应原理不一样,故速率不相等,错误;C、速率为 ="5.0" ×10-5mol·L-1·s-1,正确;D、55℃时,没有出现蓝色,故淀粉已不能作为该反应的指示剂,正确。
="5.0" ×10-5mol·L-1·s-1,正确;D、55℃时,没有出现蓝色,故淀粉已不能作为该反应的指示剂,正确。
【考点定位】
A、从图像中可以看出,40℃以前,温度越高,反应速度越快,40℃后温度越高,变色时间越长,反应越慢,而55℃,未变蓝,说明没有生成I2,正确;B、b、c点对应的反应原理不一样,故速率不相等,错误;C、速率为
 ="5.0" ×10-5mol·L-1·s-1,正确;D、55℃时,没有出现蓝色,故淀粉已不能作为该反应的指示剂,正确。
="5.0" ×10-5mol·L-1·s-1,正确;D、55℃时,没有出现蓝色,故淀粉已不能作为该反应的指示剂,正确。【考点定位】

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
 NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol?L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol?L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )| A、40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 | B、图中b、c两点对应的NaHSO3反应速率相等 | C、图中a点对应的NaHSO3反应速率为5.0×10-5mol?L-1?s-1 | D、温度高于40℃时,淀粉不宜用作该实验的指示剂 |
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020mol·L-1NaHSO3(含少量淀粉)10.0ml、KIO3(过量)酸性溶液40.0ml混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是
| A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 |
| B.图中b、c两点对应的NaHSO3反应速率相等 |
| C.图中a点对应的NaHSO3反应速率为5.0 ×10-5mol·L-1·s-1 |
| D.温度高于40℃时,淀粉不宜用作该试验的指示剂 |