题目内容
下列离子方式书写正确的是( )
| A、NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、向稀Fe(NO3)2和NaBr混合溶液中滴加稀盐酸6Br-+8H++2NO3-=3Br2+2NO↑+4H2O |
| C、Na2S溶液中滴加NaClO溶液:S2-+ClO-+H2O=S↓+Cl-+2OH- |
| D、双氧水使酸性KMnO4溶液褪色2MnO4-+5H2O2=2Mn2++5O2↑+6OH-+2H2O |
考点:离子方程式的书写
专题:
分析:A.二者反应生成氢氧化铝和碳酸氢钠;
B.二者反应生成铁离子、溴、NO和水;
C.二者发生氧化还原反应生成氯离子和S;
D.双氧水和酸性高锰酸钾反应生成锰离子、氧气和水.
B.二者反应生成铁离子、溴、NO和水;
C.二者发生氧化还原反应生成氯离子和S;
D.双氧水和酸性高锰酸钾反应生成锰离子、氧气和水.
解答:
解:A.二者反应生成氢氧化铝和碳酸氢钠,离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故A错误;
B.二者反应生成铁离子、溴、NO和水,离子方程式为4H++Fe2++NO3-+2Br-=Fe3++Br2+NO↑+2H2O,故B错误;
C.二者发生氧化还原反应生成氯离子和S,离子方程式为S2-+ClO-+H2O=S↓+Cl-+2OH-,故C正确;
D.双氧水和酸性高锰酸钾反应生成锰离子、氧气和水,离子方程式为5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O,故D错误;
故选C.
B.二者反应生成铁离子、溴、NO和水,离子方程式为4H++Fe2++NO3-+2Br-=Fe3++Br2+NO↑+2H2O,故B错误;
C.二者发生氧化还原反应生成氯离子和S,离子方程式为S2-+ClO-+H2O=S↓+Cl-+2OH-,故C正确;
D.双氧水和酸性高锰酸钾反应生成锰离子、氧气和水,离子方程式为5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O,故D错误;
故选C.
点评:本题考查离子方程式正误判断,侧重考查氧化还原反应、复分解反应,明确物质之间的反应及离子方程式书写规则是解本题关键,难点是B选项,注意亚铁离子、溴离子反应先后顺序,为易错点.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
用氢气还原ag氧化铜,得到bg铜,则铜的相对原子质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列溶液互滴不能鉴别的是( )
| A、碳酸钠溶液和稀盐酸 |
| B、偏铝酸钾溶液和稀硫酸 |
| C、硫酸铝溶液和氨水 |
| D、氯化铝溶液和氢氧化钡溶液 |
下列表述正确的是( )
| A、常温下pH=1的一元酸和pH=13的一元碱等体积混合所得溶液一定呈中性 |
| B、常温下,pH=7的氨水与氯化铵的混合溶液中,Cl-与NH4+的浓度关系c(Cl-)>c(NH4+) |
| C、10mL 0.10mol?L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是C(Na+)>C(CH3COO-)>C(OH-)>C(H+) |
| D、中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
下列实验不能达到目的是( )
| A、往酸性KMnO4溶液中通入乙烯验证乙烯的还原性 |
| B、加热氯化铵与氢氧化钙固体混合物制取氨气 |
| C、用二氧化锰和稀盐酸反应制取氯气 |
| D、用四氯化碳萃取碘水中的碘 |
有关物质的检验,以下说法正确的是( )
| A、某气体可以使燃着的木条熄灭,说明该气体是CO2 |
| B、向某溶液中滴加AgNO3溶液,有生成白色,说明原溶液中含有Cl- |
| C、向某溶液中滴加用HNO3酸化的AgNO3溶液有白色沉淀产生,说明原溶液中含有Cl- |
| D、向某溶液中滴加BaCl2溶液,有白色沉淀产生,说明原溶液中可能存在CO32-或者SO42 |
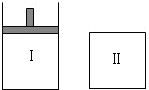 如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器.其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器.其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )| A、若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅱ>Ⅰ |
| B、若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| C、若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间相同 |
| D、平衡时Ⅰ容器的体积小于V L |