��Ŀ����
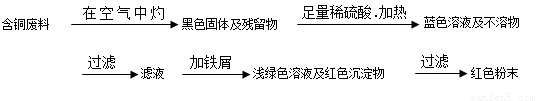
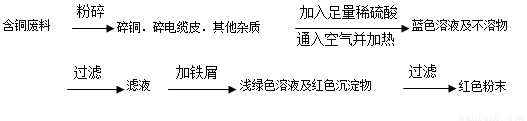
�Ȼ�ͭ�����г���FeC12���ʣ�Ϊ�Ƶô����Ȼ�ͭ���壨CuC12?2H2O�������Ƚ�������ϡ�����У�Ȼ��������ʾ������������ᴿ��
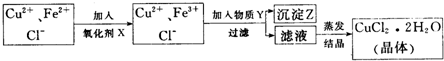
��֪����1�����������У����ʺ���Ϊ������X����
A��H2O2B��KMnO4C��NaC1O D��Ũ����
д������X������Ӧ���ӵķ���ʽ
��2�����������Y������
��3��ijͬѧ���÷�ӦCu+2H+ Cu2++H2�����ʵ����
��ȡ�Ȼ�ͭ��Һ����ͬѧ��Ƶ�װ��Ӧ��Ϊ
��4����CuC12ϡ��Һ�еõ�CuC12?2H2O���壬�������ᾧ�Ĺ����У�Ϊ�˷�ֹCu2+��ˮ�⣬Ӧ��ȡ�Ĵ�ʩ��

| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
A
A
������ţ�A��H2O2B��KMnO4C��NaC1O D��Ũ����
д������X������Ӧ���ӵķ���ʽ
2Fe2++H2O2+2H+2Fe3++2H2O
2Fe2++H2O2+2H+2Fe3++2H2O
����2�����������Y������
CuO��Cu��OH��2��CuCO3
CuO��Cu��OH��2��CuCO3
��Ŀ����������Һ��pH��ֻ����Fe��OH��3����
������Һ��pH��ֻ����Fe��OH��3����
��3��ijͬѧ���÷�ӦCu+2H+ Cu2++H2�����ʵ����
��ȡ�Ȼ�ͭ��Һ����ͬѧ��Ƶ�װ��Ӧ��Ϊ
����
����
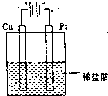
���ԭ��ء����ء������뻭����ͬѧ��Ƶ�װ��ͼ����ָ���缫���Ϻ͵������Һ����4����CuC12ϡ��Һ�еõ�CuC12?2H2O���壬�������ᾧ�Ĺ����У�Ϊ�˷�ֹCu2+��ˮ�⣬Ӧ��ȡ�Ĵ�ʩ��
��HCl�����¼���Ũ������ȴ�ᾧ
��HCl�����¼���Ũ������ȴ�ᾧ
����������1����������������Fe2+����ΪFe3+���׳�ȥ������ʱ�����������µ����ʣ�˫��ˮ����ɫ��������
��2������pH��4��5��ʹFe3+ȫ��������ͬ�������������ʣ��ݴ���ѡ����ʵ����ʣ�
��3����һ�������£�Cu�����Ӧ��Ϊʹ��ӦCu+2H+�TCu2++H2��������Ӧ��Ƴɵ��أ�ͭΪ������
��4��CuCl2��Һ�������ᾧ�����з���ˮ�⣬��ˮ��ƽ���ƶ��ĽǶȷ�����
��2������pH��4��5��ʹFe3+ȫ��������ͬ�������������ʣ��ݴ���ѡ����ʵ����ʣ�
��3����һ�������£�Cu�����Ӧ��Ϊʹ��ӦCu+2H+�TCu2++H2��������Ӧ��Ƴɵ��أ�ͭΪ������
��4��CuCl2��Һ�������ᾧ�����з���ˮ�⣬��ˮ��ƽ���ƶ��ĽǶȷ�����
��� �⣺��1�����ݿ�ͼ������������X�ɰ�Fe2+����ΪFe3+����û�����������ʣ�����XΪH2O2�������ķ�ӦΪ��2Fe2++H2O2+2H+2Fe3++2H2O���ʴ�Ϊ��A��2Fe2++H2O2+2H+2Fe3++2H2O��
�⣺��1�����ݿ�ͼ������������X�ɰ�Fe2+����ΪFe3+����û�����������ʣ�����XΪH2O2�������ķ�ӦΪ��2Fe2++H2O2+2H+2Fe3++2H2O���ʴ�Ϊ��A��2Fe2++H2O2+2H+2Fe3++2H2O��
��2���ٽ����ʾ������pH��4��5��ʹFe3+ȫ��������ͬ�������������ʣ�����Y���ΪCuO��Cu��OH��2��CuCO3���ʴ�Ϊ��CuO��Cu��OH��2��CuCO3��
��3��Cu�������Ӧ��Ϊʹ��ӦCu+2H+�TCu2++H2��������Ӧ��Ƴɵ��أ�ͭ���������ɽ�ͭ��������̼����Ϊ����������Ϊ����ʣ���Ƶ���Ϊ ���ʴ�Ϊ�����أ�
���ʴ�Ϊ�����أ� ��
��
��4��CuCl2��Һ�������ᾧ�����з���ˮ�⣬Ϊ������ˮ�⣬����Cu2++2H2O Cu��OH��2+2H+��������������������ã�����������������Ҫ���Ͻ����Ҳ������ɣ��ʴ�Ϊ����HCl�����¼���Ũ������ȴ�ᾧ��
Cu��OH��2+2H+��������������������ã�����������������Ҫ���Ͻ����Ҳ������ɣ��ʴ�Ϊ����HCl�����¼���Ũ������ȴ�ᾧ��
 �⣺��1�����ݿ�ͼ������������X�ɰ�Fe2+����ΪFe3+����û�����������ʣ�����XΪH2O2�������ķ�ӦΪ��2Fe2++H2O2+2H+2Fe3++2H2O���ʴ�Ϊ��A��2Fe2++H2O2+2H+2Fe3++2H2O��
�⣺��1�����ݿ�ͼ������������X�ɰ�Fe2+����ΪFe3+����û�����������ʣ�����XΪH2O2�������ķ�ӦΪ��2Fe2++H2O2+2H+2Fe3++2H2O���ʴ�Ϊ��A��2Fe2++H2O2+2H+2Fe3++2H2O����2���ٽ����ʾ������pH��4��5��ʹFe3+ȫ��������ͬ�������������ʣ�����Y���ΪCuO��Cu��OH��2��CuCO3���ʴ�Ϊ��CuO��Cu��OH��2��CuCO3��
��3��Cu�������Ӧ��Ϊʹ��ӦCu+2H+�TCu2++H2��������Ӧ��Ƴɵ��أ�ͭ���������ɽ�ͭ��������̼����Ϊ����������Ϊ����ʣ���Ƶ���Ϊ
 ���ʴ�Ϊ�����أ�
���ʴ�Ϊ�����أ� ��
����4��CuCl2��Һ�������ᾧ�����з���ˮ�⣬Ϊ������ˮ�⣬����Cu2++2H2O
 Cu��OH��2+2H+��������������������ã�����������������Ҫ���Ͻ����Ҳ������ɣ��ʴ�Ϊ����HCl�����¼���Ũ������ȴ�ᾧ��
Cu��OH��2+2H+��������������������ã�����������������Ҫ���Ͻ����Ҳ������ɣ��ʴ�Ϊ����HCl�����¼���Ũ������ȴ�ᾧ�����������⿼���Ȼ�ͭ�������ȡʵ�����̣���Ŀ�Ѷ��еȣ�����ʱע��������⣬��ϸ���⣮

��ϰ��ϵ�д�
�����Ŀ