题目内容
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,3.2gO2所含的原子数为0.2NA |
| B、常温下11.2L甲烷气体所含的分子数为0.5NA |
| C、18gD2O所含的电子数为10NA |
| D、1.5molNO2与足量水反应,转移的电子数为1.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据氧气是由氧原子构成来分析;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、求出重水的物质的量,然后根据重水为10电子分子来分析;
D、NO2与水的反应为歧化反应.
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、求出重水的物质的量,然后根据重水为10电子分子来分析;
D、NO2与水的反应为歧化反应.
解答:
解:解:A、氧气是由氧原子构成的,3.2gO2所含的原子的物质的量n=
=0.2mol,即0.2NA个,故A正确;
B、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L甲烷的物质的量小于0.5mol,分子数小于0.5NA个,故B错误;
C、18g重水的物质的量n=
=0.9mol,而重水为10电子分子,故0.9mol重水中含9mol电子,故C错误;
D、NO2与水的反应为歧化反应,反应中3molNO2转移2mol电子,故1.5molNO2转移1mol电子,故D错误.
故选A.
| 3.2g |
| 16g/mol |
B、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L甲烷的物质的量小于0.5mol,分子数小于0.5NA个,故B错误;
C、18g重水的物质的量n=
| 18g |
| 20g/mol |
D、NO2与水的反应为歧化反应,反应中3molNO2转移2mol电子,故1.5molNO2转移1mol电子,故D错误.
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有机化合物的分类不正确的是( )
| 结构简式 | 物质类别 | |
| A |  | 苯的同系物 |
| B | 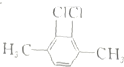 | 芳香族化合物 |
| C | 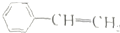 | 不饱和烃 |
| D | 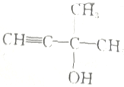 | 不饱和醇 |
| A、A | B、B | C、C | D、D |
室温下,0.1mol/L的HA溶液中
=1010.下列有关说法正确的是( )
| c(H+) |
| c(OH-) |
| A、溶液的pH=4 | ||
B、加蒸馏水稀释后,
| ||
| C、体积和pH均相等的HA与盐酸中加入足量锌,盐酸中产生的气体多 | ||
| D、在NaA溶液中存在浓度关系:c(H+)>c(OH-) |
下列化学用语表达正确的是( )
A、对硝基甲苯的结构简式: |
B、CH2F2的电子式: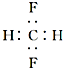 |
C、苯分子的比例模型: |
| D、16O2与18O2互为同素异形体 |
能产生丁达尔效应的分散系是( )
| A、Fe(OH)3胶体 |
| B、蒸馏水 |
| C、饱和食盐水 |
| D、纯净的空气 |
设NA代表阿伏加德罗常数的值.下列说法错误的是( )
| A、30g甲醛(CH2O)与30g葡萄糖均含有NA个碳原子 |
| B、0.1molCl2与过量稀NaOH 溶液作用转移电子数0.2NA |
| C、常温下,1L pH=1的硫酸由水电离出的H+ 约为1×10-13NA |
| D、石墨电极电解CuSO4 溶液,阴极上有4mol电子转移,阳极上有NA个O2 |
下列离子方程式书写正确的是( )
A、酸性高锰酸钾与少量双氧水反应:2MnO
| ||||
B、用石墨电极电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
C、Mg(HCO3)2溶液与过量的NaOH溶液反应:Mg2++HCO
| ||||
| D、向NaClO溶液中通入过量CO2;CO2+ClO-+H2O=HCO3-+HClO |
下列有关实验的叙述正确的是( )
| A、检验溶液中SO42-的方法是:先加入BaCl2溶液,再加盐酸 |
| B、从溴水中提纯单质溴的方法是:先用CCl4萃取,分液后再蒸馏 |
| C、证明气体分子中含有“C=C”的方法是:将该气体通入KMnO4酸性溶液 |
| D、除去CO2中少量HCl的方法是:将混合气体通过盛有饱和NaHSO3溶液的洗气瓶 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1 mol甲烷中含有10NA个质子 |
| B、27g铝被完全氧化成氧化铝,失去2NA个电子 |
| C、标准状况下,22.4 L苯含有NA个C6H6分子 |
| D、常温常压下,28g乙烯含有2NA个碳碳双键 |