题目内容
对于可逆反应X(g)+Y(g)?2Z(g),在相同温度下于四个体积相等的密闭容器内按下列配比进行反应,达到平衡时,Y所占的百分含量最低的是( )
| A、a mol X+a mol Y |
| B、2a mol Z |
| C、a mol X+a mol Z |
| D、a mol Y+a mol Z |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:根据等效平衡的思想,将生成物都折算成反应物,再进行比较,
X(g)+Y(g)?2Z(g)
A:起始(mol) a a 0
折算后(mol) a a 0
B:起始(mol) 0 0 2a
折算后(mol) a a 0
C:起始(mol) a 0 a
折算后(mol) 1.5a 0.5a 0
D:起始(mol) 0 a a
折算后(mol) 0.5a 1.5a 0
比较上面四组折算后的数据可知,A和B中Y的百分含量相等,而C中Y的百分含量低于A和B,D中的Y的百分含量高于A和B,据此答题;
X(g)+Y(g)?2Z(g)
A:起始(mol) a a 0
折算后(mol) a a 0
B:起始(mol) 0 0 2a
折算后(mol) a a 0
C:起始(mol) a 0 a
折算后(mol) 1.5a 0.5a 0
D:起始(mol) 0 a a
折算后(mol) 0.5a 1.5a 0
比较上面四组折算后的数据可知,A和B中Y的百分含量相等,而C中Y的百分含量低于A和B,D中的Y的百分含量高于A和B,据此答题;
解答:
解:根据等效平衡的思想,将生成物都折算成反应物,再进行比较,
X(g)+Y(g)?2Z(g)
A:起始(mol) a a 0
折算后(mol) a a 0
B:起始(mol) 0 0 2a
折算后(mol) a a 0
C:起始(mol) a 0 a
折算后(mol) 1.5a 0.5a 0
D:起始(mol) 0 a a
折算后(mol) 0.5a 1.5a 0
比较上面四组折算后的数据可知,A和B中Y的百分含量相等,而C中Y的百分含量低于A和B,D中的Y的百分含量高于A和B,故答案选C;
X(g)+Y(g)?2Z(g)
A:起始(mol) a a 0
折算后(mol) a a 0
B:起始(mol) 0 0 2a
折算后(mol) a a 0
C:起始(mol) a 0 a
折算后(mol) 1.5a 0.5a 0
D:起始(mol) 0 a a
折算后(mol) 0.5a 1.5a 0
比较上面四组折算后的数据可知,A和B中Y的百分含量相等,而C中Y的百分含量低于A和B,D中的Y的百分含量高于A和B,故答案选C;
点评:本题主要考查了等效平衡的思想,难度不大,注意物质之间的换算.

练习册系列答案
相关题目
为了萃取碘水中的碘,不能选用的萃取剂是( )
| A、CCl4 |
| B、汽油 |
| C、苯 |
| D、酒精 |
可用来制取硅酸的反应是( )
| A、硅酸钙中加入稀硫酸 |
| B、二氧化硅加入沸水中 |
| C、水玻璃中通入足量CO2 |
| D、硅酸钠溶液中加入盐酸 |
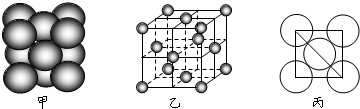
 如图所示的3种有机物中,●表示一个碳原子,氢原子未画出,则它们互为( )
如图所示的3种有机物中,●表示一个碳原子,氢原子未画出,则它们互为( )| A、同位素 | B、同系物 |
| C、同分异构体 | D、同素异形体 |
下列有关实验的叙述,正确的是( )
| A、乙烷和氯气光照下制取纯净的氯乙烷 |
| B、用分液漏斗分离环己烷和水的混合液体 |
| C、用浓氨水洗涤做过银镜反应的试管 |
| D、在苯和溴水的混合物中加入铁粉制取溴苯 |
下列说法不正确的是( )
| A、所有的化学反应都伴随着能量变化 |
| B、放热反应发生时不必加热 |
| C、化学反应的热效应数值与参加反应的物质的多少有关 |
| D、一般来说,吸热反应在一定条件下也能发生 |
下列说法不正确的是( )
| A、比较多电子原子中电子能量大小的依据是电子离原子核的远近 |
| B、各能级最多容纳的电子数是该能级原子轨道数的二倍,其理论依据是构造原理 |
| C、电子排布在同一能级时,总是自由配对,优先占据同一轨道,且自旋方向相反 |
| D、钠的焰色与原子核外电子发生跃迁有关 |