题目内容
为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)的工艺.某同学根据该原理设计的实验装置如图所示:

请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为 ;
装置B中碱石灰的作用是 .
(2)反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收;二是 .
(3)装置D的试管中产生的现象是 .
(4)取下装置E,并将烧杯中溶液倒入蒸发皿中,微火小心蒸干得到固体样品(此温度下铵盐不分解).称取不同质量的上述固体样品分别与16.00mL相同浓度的氢氧化钠溶液混合,完全溶解后,加热充分反应,并使放出的氨气全部被稀硫酸吸收,测得氨气的质量.部分实验数据如下:
①所用氢氧化钠溶液的物质的量浓度为 mol?L-1;
②a= .

请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为
装置B中碱石灰的作用是
(2)反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收;二是
(3)装置D的试管中产生的现象是
(4)取下装置E,并将烧杯中溶液倒入蒸发皿中,微火小心蒸干得到固体样品(此温度下铵盐不分解).称取不同质量的上述固体样品分别与16.00mL相同浓度的氢氧化钠溶液混合,完全溶解后,加热充分反应,并使放出的氨气全部被稀硫酸吸收,测得氨气的质量.部分实验数据如下:
| NaOH溶液的体积/mL | 16.00 | |||
| 样品的质量/g | 3.1 | 6.2 | 9.3 | 12.4 |
| 氨气的质量/g | 0.748 | 0.748 | 0.680 | a |
②a=
考点:制备实验方案的设计,镁、铝的重要化合物
专题:几种重要的金属及其化合物
分析:利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl),为了使反应产生的氨气完全导出并被稀硫酸充分吸收,并还能防止装置D中的氯化铝溶液倒吸入装置C,反应过程中持续通入N2,氨气极易溶于水,可以用碱石灰来吸收,氨水可以和氯化铝之间反应生成氢氧化铝,氨气的尾气处理用硫酸即可.
(1)根据题目信息:利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)来书写化学方程式即可;
(2)根据实验过程中氮气不会好其他物质间产生任何化学反应以及大气压强原理来回答;
(3)氨水可以和氯化铝之间反应,产生白色沉淀氢氧化铝;
(4)根据硫酸氢铵、硫酸铵和氢氧化钠之间的量的关系来计算.
(1)根据题目信息:利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)来书写化学方程式即可;
(2)根据实验过程中氮气不会好其他物质间产生任何化学反应以及大气压强原理来回答;
(3)氨水可以和氯化铝之间反应,产生白色沉淀氢氧化铝;
(4)根据硫酸氢铵、硫酸铵和氢氧化钠之间的量的关系来计算.
解答:
解:(1)根据题意:利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl),发生的反应为:Mg(OH)2+NH4Cl
MgOHCl+NH3↑+H2O,碱石灰可以用来干燥氨气,故答案为:Mg(OH)2+NH4Cl
MgOHCl+NH3↑+H2O;干燥氨气;
(2)由于氨气是极易溶于水的,反应过程中持续通入N2,可以使反应产生的氨气完全导出并被稀硫酸充分吸收,并还能防止装置D中的氯化铝溶液倒吸入装置C,故答案为:防止装置D中的氯化铝溶液倒吸入装置C;
(3)在D中,氨可以和氯化铝之间反应,产生白色沉淀氢氧化铝,产生的白色沉淀不会溶解,故答案为:产生白色沉淀;
(4)①由表中氨气质量随着样品质量的增加而下降可以知道:样品中含有硫酸氢铵和硫酸铵,样品质量是3.1g时,设含有的硫酸氢铵和硫酸铵的物质的量分别是x和y,则x+2y=
=0.044mol,115x+132y=3.1,解得x=0.004mol,y=0.02mol,氢氧化钠中和硫氢化钠溶液中的H+,余下
=0.04mol氢氧化钠和铵根离子反应生成氨气,故n(NaOH)=0.052mol,c(NaOH)=
=3.25mol/L,
故答案为:3.25;
②12.4g样品中含有硫酸氢铵和硫酸铵的物质的量分别是0.016mol和0.08mol.0.016mol氢氧化钠中和硫酸氢钠中的氢离子,余下0.052mol-0.016mol=0.036mol氢氧化钠和氨根离子反应产生氨气,即氨气的质量是0.036mol×17g/mol=0.612g,故答案为:0.612.
| ||
| ||
(2)由于氨气是极易溶于水的,反应过程中持续通入N2,可以使反应产生的氨气完全导出并被稀硫酸充分吸收,并还能防止装置D中的氯化铝溶液倒吸入装置C,故答案为:防止装置D中的氯化铝溶液倒吸入装置C;
(3)在D中,氨可以和氯化铝之间反应,产生白色沉淀氢氧化铝,产生的白色沉淀不会溶解,故答案为:产生白色沉淀;
(4)①由表中氨气质量随着样品质量的增加而下降可以知道:样品中含有硫酸氢铵和硫酸铵,样品质量是3.1g时,设含有的硫酸氢铵和硫酸铵的物质的量分别是x和y,则x+2y=
| 0.748g |
| 17g/mol |
| 0.68g |
| 17g/mol |
| 0.052mol |
| 0.016L |
故答案为:3.25;
②12.4g样品中含有硫酸氢铵和硫酸铵的物质的量分别是0.016mol和0.08mol.0.016mol氢氧化钠中和硫酸氢钠中的氢离子,余下0.052mol-0.016mol=0.036mol氢氧化钠和氨根离子反应产生氨气,即氨气的质量是0.036mol×17g/mol=0.612g,故答案为:0.612.
点评:本题是一道实验方案设计的考查题,要求学生具有的分析和解决问题的能力,难度大.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
为实现“绿色奥运”,下列建议不合理的是( )
| A、推广使用无磷洗涤剂 |
| B、推广垃圾分类存放、回收和处理 |
| C、提倡使用手帕,减少餐巾纸的使用 |
| D、提倡使用一次性塑料餐具和塑料袋 |
向某溶液中滴入无色酚酞,溶液呈红色.下列离子在该溶液中一定能生成沉淀的是( )
| A、Na+ |
| B、Cl- |
| C、Fe3+ |
| D、SO42- |


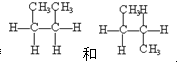


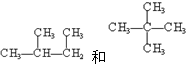




 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.
 下列物质A~F是我们熟悉的单质或化合物,其中A是一种常见的金属;B常温下是黄绿色气体;单质C含有的元素是位于元素周期表中第一周期ⅠA族; E是无色溶液.在适当的条件下,它们可以按下面框图进行反应.
下列物质A~F是我们熟悉的单质或化合物,其中A是一种常见的金属;B常温下是黄绿色气体;单质C含有的元素是位于元素周期表中第一周期ⅠA族; E是无色溶液.在适当的条件下,它们可以按下面框图进行反应. ③CH3CHO、④CH3COOH中,俗称醋酸的是
③CH3CHO、④CH3COOH中,俗称醋酸的是