题目内容
8.下列离子方程式书写正确的是( )| A. | 硫酸亚铁加过氧化氢溶液:Fe2++H2O2+2H+═Fe3++4H2O | |
| B. | 将少量硝酸银溶液滴入氨水中:Ag++2NH3•H2O═[Ag(NH3)2]++2H2O | |
| C. | KAl(SO4)2中滴加Ba(OH)2使SO42-恰好完全沉淀:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 铝粉与NaOH的溶液反应:2Al+2OH-═AlO2-+H2↑ |
分析 A.电子、电荷不守恒;
B.反应生成银氨溶液;
C.SO42-恰好完全沉淀,反应生成硫酸钡和偏铝酸钾;
D.漏写氧化剂水.
解答 解:A.硫酸亚铁加过氧化氢溶液的离子反应为2Fe2++H2O2+2H+═2Fe3++2H2O,故A错误;
B.将少量硝酸银溶液滴入氨水中的离子反应为Ag++2NH3•H2O═[Ag(NH3)2]++2H2O,故B正确;
C.KAl(SO4)2中滴加Ba(OH)2使SO42-恰好完全沉淀的离子反应为Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O,故C错误;
D.铝粉与NaOH的溶液反应的离子反应为2H2O+2Al+2OH-═2AlO2-+3H2↑,故D错误;
故选B.
点评 本题考查离子反应书写的正误判断,为高频考点,把握常见离子之间的反应为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
18.某共价化合物含碳、氢、氮三种元素,分子内有四个氮原子,且四个氮原子构成正四面体(如白磷结构)每两个氮原子间都有一个碳原子.已知分子内无碳碳单键,也没有碳碳双键,则该化合物的分子式为( )
| A. | C6H12N4 | B. | C4H8N4 | C. | C6H10N4 | D. | C6H8N4 |
19.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于元素周期表的P区;溴的价电子排布式为4S24P5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写出名称).
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图1I、II所示:
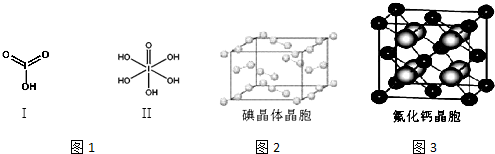
请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出一个ClO2-的等电子体Cl2O.
(6)图2为碘晶体晶胞结构.有关说法中正确的是AD.
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(7)已知CaF2晶体(见图3)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{{a}^{3}ρ{N}_{A}}{4}$.
(1)卤族元素位于元素周期表的P区;溴的价电子排布式为4S24P5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写出名称).
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |

请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出一个ClO2-的等电子体Cl2O.
(6)图2为碘晶体晶胞结构.有关说法中正确的是AD.
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(7)已知CaF2晶体(见图3)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{{a}^{3}ρ{N}_{A}}{4}$.
16.下列物质只含有共价键的化合物是( )
| A. | N2 | B. | NaOH | C. | H2O | D. | Ar |
3.下列实验操作中错误的是( )
| A. | 进行蒸发操作时,当溶液中出现较多固体时即可停止加热 | |
| B. | 进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
20.下列实验操作或叙述正确的是(填序号)( )
| A. | 乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇 | |
| B. | 将无水乙醇和浓硫酸按体积比3:1混合,加热至170℃制取乙烯 | |
| C. | 蔗糖水解用浓硫酸作催化剂 | |
| D. | 油脂皂化反应后,反应混合物中加入食盐可将肥皂分离出来 |
17.生产、生活离不开化学.下列说法中不正确的是( )
| A. | 油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 | |
| B. | 加热能杀死甲型 HINI 流感病毒是因为病毒的蛋白质受热变性 | |
| C. | 利用太阳能等能源替代化石能源能改善空气质量 | |
| D. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
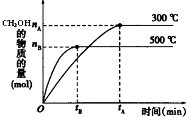 一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.
一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.