题目内容
S、Cl、Fe等元素都是中学化学中的重要元素,它们的单质及其化合物都有广泛的用途.
(1)固体硫的晶体类型是 .S原子的原子结构示意图为
(2)Na2S的电子式为
(3)用Fe3+的盐溶液做刻蚀液可将试管中的银镜洗去.
①用FeCl3溶液清洗银镜比用Fe(NO3)3溶液快,FeCl3溶液清洗银镜的离子方程式:
②欲从洗银废液(Fe2+、Ag+、NO3-)中回收银和刻蚀液,设计了如下路线:
a.过程I中反应的离子方程式是

b.过程Ⅱ中加入的试剂可以是 .
(4)某同学欲对用ClO2消毒过的水进行Cl-含量的测定.实验过程如下:向30.00mL水样中加几滴K2CrO4溶液作指示剂,用0.001000mol/LAgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达到滴定终点,此时用去AgNO3溶液12.12mL,则:
①水样中Cl-的物质的量浓度是 ;
②如在滴定终点时,测得溶液中的CrO42-浓度是3.000×10-3mol/L,则此时溶液中Cl-的浓度为 .(已知Ksp(AgCl)=1.77×10-10,Ksp(Ag2CrO4)=2.70×10-12)
(1)固体硫的晶体类型是
(2)Na2S的电子式为
(3)用Fe3+的盐溶液做刻蚀液可将试管中的银镜洗去.
①用FeCl3溶液清洗银镜比用Fe(NO3)3溶液快,FeCl3溶液清洗银镜的离子方程式:
②欲从洗银废液(Fe2+、Ag+、NO3-)中回收银和刻蚀液,设计了如下路线:
a.过程I中反应的离子方程式是

b.过程Ⅱ中加入的试剂可以是
(4)某同学欲对用ClO2消毒过的水进行Cl-含量的测定.实验过程如下:向30.00mL水样中加几滴K2CrO4溶液作指示剂,用0.001000mol/LAgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达到滴定终点,此时用去AgNO3溶液12.12mL,则:
①水样中Cl-的物质的量浓度是
②如在滴定终点时,测得溶液中的CrO42-浓度是3.000×10-3mol/L,则此时溶液中Cl-的浓度为
考点:含硫物质的性质及综合应用,氯、溴、碘及其化合物的综合应用,铁盐和亚铁盐的相互转变
专题:计算题,元素及其化合物
分析:(1)固体硫是非金属单质属于分子晶体;硫是16号元素,依据原子结构示意图书写;
(2)硫化钠是离子化合物,写出对应电子式;
(3)①洗银废液(Fe3+、Fe2+、Ag+、NO3-)中回收银和刻蚀液需要先加入过量铁还原Fe3+、Ag+;
②试剂Ⅱ是溶解过量的铁;
(4)①由利用Ag++Cl-=AgCl↓计算水样中Cl-的物质的量及其浓度;
②当有砖红色Ag2CrO4沉淀出现时,达滴定终点,利用Ksp(Ag2CrO4)计算c(Ag+),再利用Ksp(AgCl)计算此时溶液中Cl-的浓度.
(2)硫化钠是离子化合物,写出对应电子式;
(3)①洗银废液(Fe3+、Fe2+、Ag+、NO3-)中回收银和刻蚀液需要先加入过量铁还原Fe3+、Ag+;
②试剂Ⅱ是溶解过量的铁;
(4)①由利用Ag++Cl-=AgCl↓计算水样中Cl-的物质的量及其浓度;
②当有砖红色Ag2CrO4沉淀出现时,达滴定终点,利用Ksp(Ag2CrO4)计算c(Ag+),再利用Ksp(AgCl)计算此时溶液中Cl-的浓度.
解答:
解:(1)固体硫是非金属单质属于分子晶体;硫是16号元素,依据原子结构示意图书写为: ,故答案为:分子晶体;
,故答案为:分子晶体; ;
;
(2)Na2S的电子式为: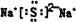 ,故答案为:
,故答案为: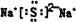 ;
;
(3)①洗银废液(Fe3+、Fe2+、Ag+、NO3-)中回收银和刻蚀液需要先加入过量铁还原Fe3+、Ag+;反应的离子方程式为:2Fe3++Fe=3Fe2+,Fe+2Ag+=Fe2++2Ag;
故答案为:2Fe3++Fe=3Fe2+,Fe+2Ag+=Fe2++2Ag;
②过程Ⅱ中加入的试剂是溶解过量的铁,可以用稀盐酸或稀硫酸;
故答案为:稀盐酸或稀硫酸;
(4)①由Ag++Cl-=AgCl↓可知,n(Cl-)=12.12×0.001L×0.001000mol?L-1=12.12×10-6mol,所以水样中c(Cl-)=
=4.04×10-4 mol?L-1,
故答案为:4.04×10-4 mol?L-1;
②当c(CrO42-)=3.00×10-3 mol?L-1出现砖红色沉淀时,由Ksp(Ag2CrO4)和 c(CrO42-)=3.00×10-3,得c(Ag+)=
=3.00×10-5 mol?L-1,
所以c(Cl-)=
=5.9×10-6 mol?L-1,故答案为:5.9×10-6 mol?L-1.
 ,故答案为:分子晶体;
,故答案为:分子晶体; ;
;(2)Na2S的电子式为:
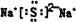 ,故答案为:
,故答案为: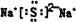 ;
;(3)①洗银废液(Fe3+、Fe2+、Ag+、NO3-)中回收银和刻蚀液需要先加入过量铁还原Fe3+、Ag+;反应的离子方程式为:2Fe3++Fe=3Fe2+,Fe+2Ag+=Fe2++2Ag;
故答案为:2Fe3++Fe=3Fe2+,Fe+2Ag+=Fe2++2Ag;
②过程Ⅱ中加入的试剂是溶解过量的铁,可以用稀盐酸或稀硫酸;
故答案为:稀盐酸或稀硫酸;
(4)①由Ag++Cl-=AgCl↓可知,n(Cl-)=12.12×0.001L×0.001000mol?L-1=12.12×10-6mol,所以水样中c(Cl-)=
| 12.12×10-6 |
| 30×10-3 |
故答案为:4.04×10-4 mol?L-1;
②当c(CrO42-)=3.00×10-3 mol?L-1出现砖红色沉淀时,由Ksp(Ag2CrO4)和 c(CrO42-)=3.00×10-3,得c(Ag+)=
|
所以c(Cl-)=
| 1.77×10-10 |
| 3.00×10-5 |
点评:本题考查了物质性质的分析应用,主要是结构分析,离子方程式书写,沉淀溶解平的计算和溶度积常数的理解应用,题目难度中等.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列装置不能达到实验目的是( )
A、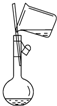 向容量瓶中转移液体 |
B、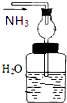 吸收NH3 |
C、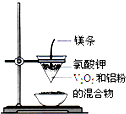 制取金属钒 |
D、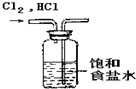 除去氯气中的氯化氢 |
 近年来,全球气候变暖给人类生存和发展带来了严峻的挑战,在此背景下,“新能源”、“低碳”、“节能减排”、“吃干榨尽”等概念愈来愈受到人们的重视.下列有关说法不正确的( )
近年来,全球气候变暖给人类生存和发展带来了严峻的挑战,在此背景下,“新能源”、“低碳”、“节能减排”、“吃干榨尽”等概念愈来愈受到人们的重视.下列有关说法不正确的( )| A、太阳能、地热能、生物质能和核聚变能均属于“新能源” |
| B、“低碳”是指采用含碳量低的烃类作为燃料 |
| C、如图甲烷经一氯甲烷生成低碳烯烃的途径体现了“节能减排”思想 |
| D、让煤变成合成气,把煤“吃干榨尽”,实现了煤的清洁、高效利用 |

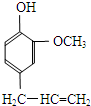 某有机化合物A因其具有麻醉作用,常用作局部麻醉剂和镇痛剂.它的结构简式如右图所示,请回答:
某有机化合物A因其具有麻醉作用,常用作局部麻醉剂和镇痛剂.它的结构简式如右图所示,请回答:
 如图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系.其中A点表示的单质是
如图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系.其中A点表示的单质是