题目内容
19.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 能使甲基橙变红的溶液:Mg2+、Na+、NO3-、Cl- | |
| B. | 0.1mol•L-1NH4Cl溶液:K+、Ba2+、OH-、CO32- | |
| C. | 0.1mol•L-1Fe(NO3)2溶液:H+、Al3+、SO42-、I- | |
| D. | 由水电离产生的c(H+)=10-12mol•L-1的溶液:NH4+、SO42-、HCO3-、Cl- |
分析 A.能使甲基橙变红的溶液呈酸性,四种离子之间不反应,都不与酸性溶液中的氢离子反应;
B.氯化铵与氢氧根离子反应,钡离子与碳酸根离子反应;
C.酸性条件下硝酸根离子具有强氧化性,能够氧化亚铁离子、碘离子;
D.由水电离产生的c(H+)=10-12mol•L-1的溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子与氢离子、氢氧根离子反应.
解答 解:A.能使甲基橙变红的溶液中存在大量氢离子,Mg2+、Na+、NO3-、Cl-之间不反应,都不与氢离子反应,在溶液中能够大量共存,故A正确;
B.Ba2+、CO32-之间反应生成碳酸钡沉淀,OH-、NH4Cl之间发生反应,在溶液中不能大量共存,故B错误;
C.Fe(NO3)2在溶液中电离出亚铁离子和硝酸根离子,硝酸根离子在酸性条件下能够氧化Fe2+、I-,在溶液不能大量共存,故C错误;
D.由水电离产生的c(H+)=10-12mol•L-1的溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,HCO3-与氢离子和氢氧根离子反应,在溶液中一定不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.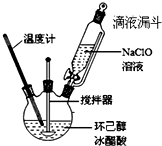 环己酮是重要的化工原料,也是重要的工业溶剂,实验室常用次氯酸氧化法制备环己酮.
环己酮是重要的化工原料,也是重要的工业溶剂,实验室常用次氯酸氧化法制备环己酮.
反应原理: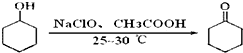
步骤:
①在如如图所示装置中,加入环己醇5.2mL(0.05mol)和冰醋酸33mL,开动电动搅拌器,将NaClO溶液缓慢滴加到反应液中,反应液温度保持在25~30℃,边加边反应,直至用KI淀粉试纸检验呈蓝色.
②一段时间后,反应液中加入足量饱和NaHSO3溶液,并将其转入250mL蒸馏烧瓶中,加入3g AlCl3和几粒沸石,摇匀.加热蒸馏至无油珠滴出为止.
③取馏出液,加入无水碳酸钠,至刚好呈碱性.继续搅拌,加入NaCl固体至不再溶解,分液取有机相.
④向有机相中加入无水硫酸镁,转入50mL蒸馏烧瓶中,馏取155.6℃左右的组分.得2.94g纯净的环己酮.
回答下列问题:
(1)该反应是放热反应,为防止温度过高可以采用的方法有控制滴加速度、冰水浴等.(任写一条)
(2)氧化法制备环己酮起氧化作用的是次氯酸,请写出NaClO和CH3COOH反应生成次氯酸的离子方程式:ClO-+CH3COOH=HClO+CH3COO-.
(3)加入饱和NaHSO3溶液的作用是除去过量的NaClO.加入NaCl固体的作用是减小环己酮的溶解度.分液时用到的玻璃仪器有分液漏斗、烧杯.
(4)蒸馏时加入AlCl3固体的作用是防起泡,加入沸石的作用是防止暴沸.上述实验中使用到滴液漏斗,相比于分液漏斗,它的优点是可以使漏斗内液体顺利流下.
(5)计算本实验的产率60%.
(6)第②步中,设计实验证明:加入的饱和NaHSO3溶液已经足量.取一段KI淀粉试纸于表面皿上,用玻璃棒蘸取反应液点试纸中央,若不变蓝,则NaHSO3溶液已足量.
 环己酮是重要的化工原料,也是重要的工业溶剂,实验室常用次氯酸氧化法制备环己酮.
环己酮是重要的化工原料,也是重要的工业溶剂,实验室常用次氯酸氧化法制备环己酮.反应原理:
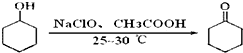
| 物质 | 熔点(℃) | 沸点(℃) | 溶解性 |
| 环己醇 | 26 | 160.8 | 可溶于水 |
| 环己酮 | -45 | 155.6 | 微溶于水 |
| 冰醋酸 | 16.6 | 117.9 | 可溶于水 |
①在如如图所示装置中,加入环己醇5.2mL(0.05mol)和冰醋酸33mL,开动电动搅拌器,将NaClO溶液缓慢滴加到反应液中,反应液温度保持在25~30℃,边加边反应,直至用KI淀粉试纸检验呈蓝色.
②一段时间后,反应液中加入足量饱和NaHSO3溶液,并将其转入250mL蒸馏烧瓶中,加入3g AlCl3和几粒沸石,摇匀.加热蒸馏至无油珠滴出为止.
③取馏出液,加入无水碳酸钠,至刚好呈碱性.继续搅拌,加入NaCl固体至不再溶解,分液取有机相.
④向有机相中加入无水硫酸镁,转入50mL蒸馏烧瓶中,馏取155.6℃左右的组分.得2.94g纯净的环己酮.
回答下列问题:
(1)该反应是放热反应,为防止温度过高可以采用的方法有控制滴加速度、冰水浴等.(任写一条)
(2)氧化法制备环己酮起氧化作用的是次氯酸,请写出NaClO和CH3COOH反应生成次氯酸的离子方程式:ClO-+CH3COOH=HClO+CH3COO-.
(3)加入饱和NaHSO3溶液的作用是除去过量的NaClO.加入NaCl固体的作用是减小环己酮的溶解度.分液时用到的玻璃仪器有分液漏斗、烧杯.
(4)蒸馏时加入AlCl3固体的作用是防起泡,加入沸石的作用是防止暴沸.上述实验中使用到滴液漏斗,相比于分液漏斗,它的优点是可以使漏斗内液体顺利流下.
(5)计算本实验的产率60%.
(6)第②步中,设计实验证明:加入的饱和NaHSO3溶液已经足量.取一段KI淀粉试纸于表面皿上,用玻璃棒蘸取反应液点试纸中央,若不变蓝,则NaHSO3溶液已足量.
7.合成氨是工业上的重要反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g),下列说法不正确的是( )
| A. | 反应达到平衡状态后,各物质浓度不变,反应停止 | |
| B. | 反应达到平衡状态后,单位时间内生成1molN2的同时消耗3molH2 | |
| C. | 在上述条件下,N2不可能100%转化为NH3 | |
| D. | 使用催化剂是为了加快反应速率,提高生产效率 |
14.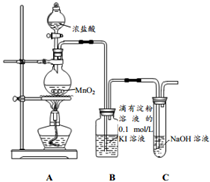 探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)
探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)
(1)装置A中生成氯气的化学反应方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)装置C中NaOH的作用是吸收多余氯气,防止污染环境;其中发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(3)能证明氯气的氧化性强于碘的实验现象是B装置中通氯气后溶液变蓝.
(4)为探究B中溶液颜色变化的原因,该小组同学查阅资料并进行实验.
查阅资料:
I2和I-在溶液中会发生反应:I2+I-?I3-,I3-显棕黄色且遇淀粉变蓝;I2可被氯气与氧化为ICl2-(红色)和ICl4-(黄色),两种离子可继续被氧化成IO3-(无色).
进行实验:
①操作Ⅰ的实验目的是证明反应后的B溶液中有淀粉,无I3-,说明溶液的浅棕色不是I3-造成的.
②写出ICl2-在水溶液中与氯气反应生成IO3-的离子方程式ICl2-+2Cl2+3H2O=IO3-+6Cl-+6H+.
③由以上实验可推断B中溶液颜色变成浅棕色的原因是I-先被氯气氧化成I2,I2又被氯气氧化成ICl2-(红色)和ICl4-(黄色),两者混合呈浅棕色溶液.
 探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)
探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)| 实验操作 | 实验现象 |
| 打开A中分液漏斗活塞,放下部分浓盐酸,加热 | 装置B中溶液变蓝色,随后蓝色褪去,溶液显浅棕色 |
(2)装置C中NaOH的作用是吸收多余氯气,防止污染环境;其中发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(3)能证明氯气的氧化性强于碘的实验现象是B装置中通氯气后溶液变蓝.
(4)为探究B中溶液颜色变化的原因,该小组同学查阅资料并进行实验.
查阅资料:
I2和I-在溶液中会发生反应:I2+I-?I3-,I3-显棕黄色且遇淀粉变蓝;I2可被氯气与氧化为ICl2-(红色)和ICl4-(黄色),两种离子可继续被氧化成IO3-(无色).
进行实验:
| 实验操作 | 实验现象 |
| Ⅰ.取反应后B中的溶液4mL分成两等份,第一份滴入1滴碘水;第二份滴入淀粉溶液 | 第一份溶液蓝色 第二份溶液颜色没有变化 |
| Ⅱ.将I2溶于KI溶液中配制得碘总浓度为0.1mol/L的溶液,取上述溶液2mL,滴加1滴淀粉溶液,再通入氯气 | 加淀粉后溶液变蓝,通氯气后蓝色褪去,溶液显浅棕色 |
| Ⅲ.向Ⅱ所得溶液继续通入氯气 | 溶液几乎变为无色 |
②写出ICl2-在水溶液中与氯气反应生成IO3-的离子方程式ICl2-+2Cl2+3H2O=IO3-+6Cl-+6H+.
③由以上实验可推断B中溶液颜色变成浅棕色的原因是I-先被氯气氧化成I2,I2又被氯气氧化成ICl2-(红色)和ICl4-(黄色),两者混合呈浅棕色溶液.
4.下列有关说法正确的是( )
| A. | 1mol过氧化钠和足量水充分反应,理论上转移的电子数约为2×6.02×1023 | |
| B. | 电工操作中将铝线与铜线直接相连,会导致铜线更快被氧化 | |
| C. | MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)<Ksp(MnS) | |
| D. | 0.1mol•L-1醋酸溶液pH=a,0.01mol•L-1醋酸溶液pH=b,则a+1<b |
8.设NA代表阿佛加德罗常数的值,下列说法正确的是( )
| A. | 1molNH4Cl固体中共价键总数为5NA | |
| B. | 16gO2与O3的混合物中含有NA个氧原子 | |
| C. | 向装有催化剂的密闭容器加入3molH2和1molN2,充分反应后得2NA个氨分子 | |
| D. | 18g水(H2O)含有8NA个电子 |
9.某有机物蒸气、空气燃烧时需3倍于其体积的氧气,产生2倍于其体积的CO2,该有机物是( )
| A. | CH4 | B. | C2H6 | C. | C2H5OH | D. | CH3CHO |
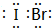 ,它是由σ键形成的(根据原子轨道的重叠程度填写).
,它是由σ键形成的(根据原子轨道的重叠程度填写).