题目内容
17.有一支盛有溶液的50ml滴定管,其液面恰好在10.00ml,现把滴定管里的溶液全部排出,用量筒承接,量筒内溶液的体积为( )| A. | 大于40.00ml | B. | 40.00ml | C. | 大于10.00ml | D. | 10.00ml |
分析 滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,量筒与此相反,据此即可解答.
解答 解:滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,50mL滴定管中实际盛放液体的体积大于50mL,因此,一支50mL滴定管中液面恰好在10mL刻度处,把管内液体全部放出,还有满刻度以下的溶液一并放出,总量超过50-10=40mL,盛入量筒内,所得液体体积一定是大于40mL,
故选A.
点评 本题考查了酸式滴定管的结构,注意滴定管的“0”刻度在上端,满刻度在下端,滴定管满刻度以下还有一段空间没有刻度,是解答的关键,题目难度不大.

练习册系列答案
相关题目
7.下列说法或表示方法中,正确的是( )
| A. | 等质量的硫蒸气和硫黄固体分别完全燃烧,前者放出的热量多 | |
| B. | a℃、b kPa下,将0.5 mol O2和1.5 mol H2置于密闭容器中充分反应生成H2O(g),放热c kJ,其热化学方程式为2H2(g)+O2(g)=2H2O(g)△H=-2c kJ•mol-1 | |
| C. | 由N2O 4(g)?2NO2(g)△H=-56.9 kJ•mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ | |
| D. | 稀硫酸溶液与稀NaOH溶液反应的中和热为57.3 kJ•mol-1,则稀醋酸溶液与稀NaOH溶液反应的热化学方程式可表示为CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)△H=-57.3 kJ•mol-1 |
8.近来雾霾频现,“PM2.5”数据监测纳入公众视野.“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒物,也称为可入肺颗粒物.下列有关说法中,错误的是( )
| A. | 雾霾有可能产生丁达尔现象 | |
| B. | “PM2.5”没有必要纳入空气质量评价指标 | |
| C. | 近年来雾霾的形成与工业排放的烟气有关系 | |
| D. | 研制开发燃料电池汽车,降低机动车尾气污染,某种程度上可以减少PM2.5污染 |
5.通常用来衡量一个国家的石油化学工业发展水平的标志是( )
| A. | 石油的需求量 | B. | 合成纤维 | C. | 石油的产量 | D. | 乙烯的产量 |
12.10mL某种气态烃,在50mL O2中完全燃烧,得到液态水和体积为35mL的混合气体(所有气体都是在常温常压下测定),则该气态烃不可能是( )
| A. | 乙烷 | B. | 丙烯(C3H6) | C. | 丁炔(C4H6) | D. | 新戊烷 |
2.能反映甲烷分子是以碳原子为中心的正四面体结构,而不是正方形平面结构的事实是( )
| A. | CH3Cl无同分异构体 | B. | CH2Cl2无同分异构体 | ||
| C. | CHCl3无同分异构体 | D. | CH4是共价化合物 |
9.下列关于钠的说法正确的是( )
| A. | 金属钠与氧气反应,条件不同,产物相同 | |
| B. | 金属钠着火可用冷水扑灭 | |
| C. | 少量的钠可保存在煤油中 | |
| D. | 钠的化学性质活泼,可从CuSO 4溶液中置换出Cu |
6.如图实验探究影响反应速率的因素是( )
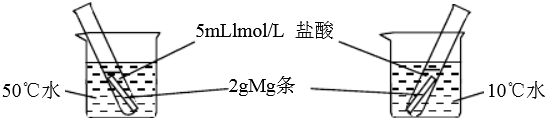

| A. | 浓度 | B. | 温度 | C. | 催化剂 | D. | 固体质量 |
7.在厦参加国际磷化学会议的科学家认为无磷洗涤剂洗涤效果差,污染更严重,建议在建立磷回收机制后,重新使用加有磷化合物的含磷洗涤剂.对此的下列说法不正确 的是( )
| A. | 含磷洗涤剂含有磷元素 | |
| B. | 只要解决污染问题,可能重新使用含磷洗涤剂 | |
| C. | 含磷洗涤剂含有磷单质 | |
| D. | 研究高效无污染的洗涤剂仍是化学家的任务 |