题目内容
15.现有三组分散系:①汽油和氯化钠溶液 ②酒精的水溶液 ③碘单质的水溶液,分离以上各混合液的正确方法依次是( )| A. | 分液、萃取、蒸馏 | B. | 分液、蒸馏、萃取 | C. | 萃取、蒸馏、分液 | D. | 蒸馏、萃取、分液 |
分析 ①汽油和氯化钠溶液,分层;
②酒精的水溶液互溶,但沸点不同;
③碘单质不易溶于水,易溶于有机溶剂.
解答 解:①汽油和氯化钠溶液,分层,选择分液法分离;
②酒精的水溶液互溶,但沸点不同,选择蒸馏法分离;
③碘单质不易溶于水,易溶于有机溶剂,则加有机溶剂(苯或四氯化碳等)萃取分离,
故选B.
点评 本题考查混合物分离提纯方法的选择,为高频考点,把握物质的性质、性质差异、混合物分离原理为解答的关键,侧重分析与应用能力的考查,注意分离原理及应用,题目难度不大.

练习册系列答案
相关题目
2.某科学探究小组为探究电化学原理,设计了如图所示的装置进行探究实验.下列对实验中观察到的现象或有关结论错误的是( )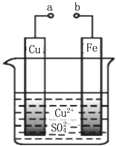

| A. | a和b不连接时,铁片上有红色的铜析出,该装置不能形成原电池 | |
| B. | a和b用导线连接时铜片为负极,发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会被氧化,溶液中均有Fe2+生成 | |
| D. | a和b用导线连接时,溶液中的Cu2+应向铜电极移动 |
3.强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、Al3+、CO32-、SO42-、Cl-中的若干种,某同学为了确认其成分,取溶液X进行连续实验,实验过程及产物如下:

下列结论正确的是( )

下列结论正确的是( )
| A. | X中肯定存在Na+、NH4+、Fe2+、Al3+、SO42- | |
| B. | 气体F经催化氧化可直接生成气体D | |
| C. | 沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH)3 | |
| D. | X中不能确定的离子是Al3+、Na+、K+和Cl- |
10.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | |
| B. | 10 mol•L-1的浓氨水:Al3+、NH4+、NO3-、I- | |
| C. | 与Al反应放出H2的溶液:Mg2+、Ca2+、HCO3-、NO3- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、Na+、AlO2-、CO32- |
20.表是元素周期表的一部分.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
(1)写出下列元素符号:①N,⑥Si.
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程: .
.
(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是H2S.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程:
 .
.(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是H2S.
 ,与N3-互为等电子体的分子为N2O(写一种);
,与N3-互为等电子体的分子为N2O(写一种);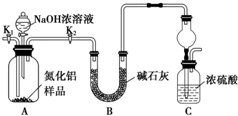
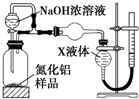
 d.NH4Cl溶液
d.NH4Cl溶液
 A、B、D、E、F五种元素的原子序数依次增大,除F为过渡元素外,其余四种均是短周期元素.已知:
A、B、D、E、F五种元素的原子序数依次增大,除F为过渡元素外,其余四种均是短周期元素.已知: