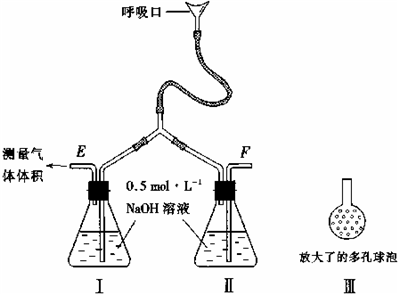
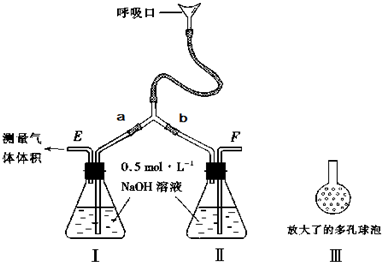
题目内容
A、B、C、D四种气体都含有氮元素.已知A能在高温高压及催化剂作用下生成B;B的水溶液是一种弱碱,B经过铂金属的催化氧化得到C;C是双原子氧化物,在空气中继续氧化得到D;D是硝酸工业尾气中有害物质之一,能与水反应生成C和一元强酸E.按要求填空(1)写出下列反应的化学方程式:
①A→B:______.
②A→C:______.
③C→D:______.
④D通入水中:______.
(2)写出强酸E与铜片反应分别生成C或D的离子方程式:
①______;
②______.
(3)B能被Cl2氧化生成A和一种铵盐,写出反应化学方程式:______.
解:A、B、C、D四种气体都含有氮元素,已知A能在高温高压及催化剂作用下生成B,B的水溶液是一种弱碱,则B是NH3,A是N2,B经过铂金属的催化氧化得到C,C是双原子氧化物,则C是NO,在空气中继续氧化得到D,D是硝酸工业尾气中有害物质之一,D是NO2,D能与水反应生成NO和一元强酸E,E是HNO3.
(1)①在高温高压催化剂条件下,氮气和氢气反应生成氨气,反应方程式为:N2+3H2 2NH3 ②氮气和氧气在放电条件下反应生成一氧化氮,反应方程式为:N2+O2
2NH3 ②氮气和氧气在放电条件下反应生成一氧化氮,反应方程式为:N2+O2 2NO,
2NO,
③一氧化氮和氧气反应生成二氧化氮,反应方程式为:2NO+O2=2NO2,④二氧化氮和水反应生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,
故答案为:①N2+3H2 2NH3,②N2+O2
2NH3,②N2+O2 2NO,③2NO+O2=2NO2,④3NO2+H2O=2HNO3+NO;
2NO,③2NO+O2=2NO2,④3NO2+H2O=2HNO3+NO;
(2)铜和稀硝酸反应生成硝酸铜、一氧化碳和水,离子反应方程式为:33Cu+2NO3-+8H+=Cu2++2NO↑+4H2O,铜和浓硝酸反应生成硝酸铜、二氧化氮和水,离子反应方程式为:
Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,
故答案为:33Cu+2NO3-+8H+=Cu2++2NO↑+4H2O,Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O;
(3)氨气和氯气反应生成氮气和氯化铵,反应方程式为:8NH3+3Cl2=N2+6NH4Cl,故答案为:8NH3+3Cl2=N2+6NH4Cl.
分析:A、B、C、D四种气体都含有氮元素,已知A能在高温高压及催化剂作用下生成B,B的水溶液是一种弱碱,则B是NH3,A是N2,B经过铂金属的催化氧化得到C,C是双原子氧化物,则C是NO,在空气中继续氧化得到D,D是硝酸工业尾气中有害物质之一,D是NO2,D能与水反应生成NO和一元强酸E,E是HNO3.
点评:本题考查了物质的推断,明确物质的性质是解本题关键,注意物质间反应条件,难度不大.
(1)①在高温高压催化剂条件下,氮气和氢气反应生成氨气,反应方程式为:N2+3H2
 2NH3 ②氮气和氧气在放电条件下反应生成一氧化氮,反应方程式为:N2+O2
2NH3 ②氮气和氧气在放电条件下反应生成一氧化氮,反应方程式为:N2+O2 2NO,
2NO,③一氧化氮和氧气反应生成二氧化氮,反应方程式为:2NO+O2=2NO2,④二氧化氮和水反应生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,
故答案为:①N2+3H2
 2NH3,②N2+O2
2NH3,②N2+O2 2NO,③2NO+O2=2NO2,④3NO2+H2O=2HNO3+NO;
2NO,③2NO+O2=2NO2,④3NO2+H2O=2HNO3+NO;(2)铜和稀硝酸反应生成硝酸铜、一氧化碳和水,离子反应方程式为:33Cu+2NO3-+8H+=Cu2++2NO↑+4H2O,铜和浓硝酸反应生成硝酸铜、二氧化氮和水,离子反应方程式为:
Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,
故答案为:33Cu+2NO3-+8H+=Cu2++2NO↑+4H2O,Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O;
(3)氨气和氯气反应生成氮气和氯化铵,反应方程式为:8NH3+3Cl2=N2+6NH4Cl,故答案为:8NH3+3Cl2=N2+6NH4Cl.
分析:A、B、C、D四种气体都含有氮元素,已知A能在高温高压及催化剂作用下生成B,B的水溶液是一种弱碱,则B是NH3,A是N2,B经过铂金属的催化氧化得到C,C是双原子氧化物,则C是NO,在空气中继续氧化得到D,D是硝酸工业尾气中有害物质之一,D是NO2,D能与水反应生成NO和一元强酸E,E是HNO3.
点评:本题考查了物质的推断,明确物质的性质是解本题关键,注意物质间反应条件,难度不大.

练习册系列答案
相关题目