题目内容
下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
填写下列空白:
(1)写出化学式:A ,B .
(2)写出反应⑤的离子方程式: .
(3)写出反应⑥的化学反应方程式: .

填写下列空白:
(1)写出化学式:A
(2)写出反应⑤的离子方程式:
(3)写出反应⑥的化学反应方程式:
考点:无机物的推断
专题:推断题
分析:A是一种常见单质,其焰色反应为黄色,则A是Na,B、C、D、E是含A元素的常见化合物,Na在O2中燃烧生成B,B为Na2O2,Na和H2O反应生成NaOH和H2,Na2O2和水反应生成NaOH和O2,所以C是NaOH,NaOH和过量CO2反应生成NaHCO3,所以E是NaHCO3,Na2O2和CO2反应生成Na2CO3和O2,NaHCO3分解生成Na2CO3、CO2和水,所以D是Na2CO3,再结合物质间的反应分析解答.
解答:
解:A是一种常见单质,其焰色反应为黄色,则A是Na,B、C、D、E是含A元素的常见化合物,Na在O2中燃烧生成B,B为Na2O2,Na和H2O反应生成NaOH和H2,Na2O2和水反应生成NaOH和O2,所以C是NaOH,NaOH和过量CO2反应生成NaHCO3,所以E是NaHCO3,Na2O2和CO2反应生成Na2CO3和O2,NaHCO3分解生成Na2CO3、CO2和水,所以D是Na2CO3,
(1)通过以上分析知,A是Na、B是Na2O2,故答案为:Na;Na2O2;
(2)NaOH和过量二氧化碳反应生成碳酸氢钠,离子方程式为:CO2+OH-=HCO3-,故答案为:CO2+OH-=HCO3-;
(3)在加热条件下,碳酸氢钠分解生成碳酸钠、二氧化碳和水,反应方程式为:2NaHCO3
Na2CO3+CO2↑+H2O,故答案为:2NaHCO3
Na2CO3+CO2↑+H2O.
(1)通过以上分析知,A是Na、B是Na2O2,故答案为:Na;Na2O2;
(2)NaOH和过量二氧化碳反应生成碳酸氢钠,离子方程式为:CO2+OH-=HCO3-,故答案为:CO2+OH-=HCO3-;
(3)在加热条件下,碳酸氢钠分解生成碳酸钠、二氧化碳和水,反应方程式为:2NaHCO3
| ||
| ||
点评:本题以钠及其化合物为载体考查了物质的推断,明确物质的性质是解本题关键,根据A为单质及焰色反应来确定A的组成,再结合物质间的反应来推断,熟悉钠及其化合物之间转化关系的网络结构,灵活运用知识解答问题,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
属于同种物质的是( )
| A、O2和O3 |
| B、12H2和13H2 |
| C、新戊烷和2,2-二甲基丙烷 |
| D、C2H5COOH与CH3COOCH3 |
已知2H2O2═2H2O+O2↑,若其他条件不变,下列措施不能使该反应速率增大的是( )
| A、降低温度 |
| B、加入少量MnO2 |
| C、加入少量FeCl3 |
| D、增大H2O2的浓度 |
在溶液中能大量共存的离子组是( )
| A、Ca2+ CO32- Cl- |
| B、H+ SO42- CO32- |
| C、K+ H+ OH- |
| D、Fe3+ Na+ NO3- |
在一定条件下,对于密闭容器中进行的反应:2SO2(g)+O2(g)?2SO3(g),下列说法能充分说明该反应已达到化学平衡状态的是( )
| A、SO2完全转化为SO3 |
| B、各物质浓度均不再改变 |
| C、SO2和SO3的浓度一定相等 |
| D、正、逆反应速率相等且等于零 |
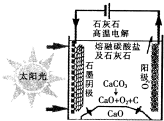 资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业
