题目内容
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3固体.相应的实验过程可用如图表示: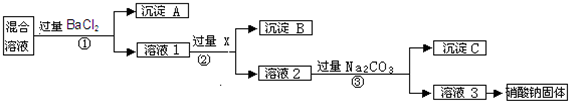
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X:
(2)上述实验流程中①②③步均要进行的实验操作是
(3)上述实验流程中加入过量的Na2CO3的目的是
(4)按此实验方案得到的溶液3中肯定含有
(5)实验室利用上述实验获得的NaNO3晶体制备480mL 0.4mol/L的NaNO3溶液:
①需要称取NaNO3固体
②实验中需要用到的玻璃仪器有烧杯、胶头滴管、玻璃棒、
分析:由流程可知,①中加氯化钡,硫酸根离子转化为沉淀,则沉淀A为BaSO4,溶液1中含氯化钠、硝酸钠、氯化钡,②中加AgNO3后氯离子转化沉淀,沉淀B为AgCl,溶液2中含硝酸钠、硝酸银、硝酸钡,③中钡离子,银离子转化为沉淀,沉淀C为碳酸钡、碳酸银,溶液3为硝酸钠和碳酸钠,转化中试剂过量保证离子完全转化为沉淀,以此来解答.
解答:解:由流程可知,①中加氯化钡,硫酸根离子转化为沉淀,则沉淀A为BaSO4,溶液1中含氯化钠、硝酸钠、氯化钡,②中加AgNO3后氯离子转化沉淀,沉淀B为AgCl,溶液2中含硝酸钠、硝酸银、硝酸钡,③中钡离子,银离子转化为沉淀,沉淀C为碳酸钡、碳酸银,溶液3为硝酸钠和碳酸钠,
(1)由上述分析可知,X为AgNO3,沉淀A为BaSO4,故答案为:AgNO3;BaSO4;
(2)流程中①②③步均生成沉淀,需要进行过滤操作,故答案为:过滤;
(3)加入过量的Na2CO3的目的是使溶液中的Ag+、Ba2+完全沉淀,故答案为:使溶液中的Ag+、Ba2+完全沉淀;
(4)溶液3中肯定含有Na2CO3,可加适量的稀硝酸后蒸发结晶或加热冷却结晶得到纯净的硝酸钠,
故答案为:Na2CO3;稀HNO3;蒸发结晶或加热冷却结晶;
(5)①制备480mL 0.4mol/L的NaNO3溶液,需要500mL容量瓶,则需要硝酸钠的质量为0.5L×0.4mol/L×85g/mol=17.0g,故答案为:17.0;
②容量瓶具有固定规格,则配制480mL还需要500mL容量瓶,故答案为:500mL容量瓶.
(1)由上述分析可知,X为AgNO3,沉淀A为BaSO4,故答案为:AgNO3;BaSO4;
(2)流程中①②③步均生成沉淀,需要进行过滤操作,故答案为:过滤;
(3)加入过量的Na2CO3的目的是使溶液中的Ag+、Ba2+完全沉淀,故答案为:使溶液中的Ag+、Ba2+完全沉淀;
(4)溶液3中肯定含有Na2CO3,可加适量的稀硝酸后蒸发结晶或加热冷却结晶得到纯净的硝酸钠,
故答案为:Na2CO3;稀HNO3;蒸发结晶或加热冷却结晶;
(5)①制备480mL 0.4mol/L的NaNO3溶液,需要500mL容量瓶,则需要硝酸钠的质量为0.5L×0.4mol/L×85g/mol=17.0g,故答案为:17.0;
②容量瓶具有固定规格,则配制480mL还需要500mL容量瓶,故答案为:500mL容量瓶.
点评:本题考查物质分离、提纯实验方案的设计,把握流程中试剂的加入发生的化学反应及操作为解答的关键,注重实验的严密性和溶液的配制、物质提纯的考查,题目难度中等.

练习册系列答案
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目