题目内容
13.下列有机溶剂中可用于贮存金属钠的是( )| A. | 汽油 | B. | 酒精 | C. | 四氯化碳 | D. | 石蜡油 |
分析 钠易与空气中的氧气、水反应,据此解题.
解答 解:A.汽油易挥发、易燃烧,所以不能将钠保存在汽油里,一般保存在煤油中,故A错误;
B.钠能与酒精反应生成氢气和乙醇钠,故B错误;
C.四氯化碳的密度大于钠,钠浮在其表面上,不能起到隔绝空气和水的作用,故C错误;
D.钠易与空气中的氧气、水等反应,与石蜡油不反应,且密度比石蜡油大,可保存在石蜡油中,故D正确.
故选D.
点评 本题考查较为综合,涉及药瓶的保存,侧重于学生的分析能力和实验能力的考查,为高频考点,注意药品的保存取决于物质的性质,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 一定条件下,1mol N2与足量H2混合反应生成NH3,转移电子数6NA | |
| B. | 在常温常压下,2.8g N2和CO的混合气体所含电子数为1.4NA | |
| C. | 标准状况下,22.4L CCl4含有的分子数目为NA | |
| D. | 在电解精炼粗铜的过程中,当转移电子数为NA时,阳极溶解32g |
1.下列溶液中,一定能大量共存的微粒组是( )
| A. | pH=1 的溶液中:K+、Fe2+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ | |
| B. | 含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO${\;}_{4}^{2-}$ | |
| C. | 25℃,由水电离出的c(H+)=1×10-13mol/L 的溶液中:K+、NH${\;}_{4}^{+}$、NO${\;}_{3}^{-}$、Cl- | |
| D. | 滴加紫色石蕊试液变红的溶液中:K+、Ba2+、Cl-、F- |
8.100mL 6mol•L-1的硫酸溶液跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,又不影响生成氢气的总量,可向反应物中加入适量的( )
| A. | Na2CO3固体 | B. | 3 mol•L-1的H2SO4溶液 | ||
| C. | CH3COOK溶液 | D. | KNO3溶液 |
18.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,5.6 LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| B. | 78 g苯含有C=C双键的数目为3 NA | |
| C. | 1 L1mol•L-1的CuSO4溶液中含NA个Cu2+ | |
| D. | 常温下,4.4gCO2和N2O混合物中所含有的原子数为0.3NA |
5.下列关于蛋白质的叙述中,不正确的是( )
| A. | 天然蛋白质的水解产物是多种a-氨基酸 | |
| B. | 蛋白质溶液里加入饱和硫酸铵溶液,蛋白质会析出,且加水也不溶解 | |
| C. | 重金属盐能使蛋白质凝结,所以误食重金属盐会中毒 | |
| D. | 浓硝酸沾到皮肤上能使浓硝酸和蛋白质发生颜色反应 |
2.下列除杂质的操作中不正确的是( )
| A. | Na2CO3 固体中混有少量NaHCO3:加热固体至质量恒定 | |
| B. | NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体 | |
| C. | CO2中混有HCl:将其通过装NaOH溶液的洗气瓶 | |
| D. | FeCl2溶液中混有少量FeCl3:加入足量铁粉,搅拌,过滤 |
3.为测定CO2的相对分子质量,某实验小组三位同学选用含NaHCO3的样品(质量均为m1g)和其它合理的试剂,进行了以下三个实验.

完成下列填空:
甲用重量法确定CO2的质量,装置如图1:
(1)B中反应的化学方程式为2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O.
(2)实验中持续缓缓通入空气,其作用之一是把生成的CO2全部排入后续装置中,使之完全被吸收;另有作用为搅拌装置B中的反应物,使之充分反应.
(3)不能提高测定精确度的措施是c.
a.向B内加入酸之前,排尽装置内的CO2气体
b.向B内滴加酸时不宜过快
c.在B、C之间增添盛有饱和NaHCO3溶液的洗气装置
d.在D后增添盛有碱石灰的干燥管
(4)乙用滴定法确定CO2的物质的量将样品配制成100mL溶液,从中取出20.00mL,用c mol•L-1的盐酸滴定(甲基橙作指示剂).当溶液由黄色变为橙色,且保持30s不变时,停止滴定.平行测定三次,有关实验数据记录如下表.m1 g样品产生CO2的物质的量为0.125cmol.
(5)丙用气体体积法确定CO2的体积,装置如右上图所示.
①为了减小实验误差,量气管中加入的液体X为饱和碳酸氢钠溶液;
②若该装置气密性良好,读数平视,但测得的“CO2体积”数据仍然偏小,其原因可能是水准管的液面高于量气管中的液面.
(6)确定CO2的相对分子质量,选用甲、乙(限用“甲”、“乙”、“丙”进行填写)的实验数据为最佳.

完成下列填空:
甲用重量法确定CO2的质量,装置如图1:
(1)B中反应的化学方程式为2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O.
(2)实验中持续缓缓通入空气,其作用之一是把生成的CO2全部排入后续装置中,使之完全被吸收;另有作用为搅拌装置B中的反应物,使之充分反应.
(3)不能提高测定精确度的措施是c.
a.向B内加入酸之前,排尽装置内的CO2气体
b.向B内滴加酸时不宜过快
c.在B、C之间增添盛有饱和NaHCO3溶液的洗气装置
d.在D后增添盛有碱石灰的干燥管
(4)乙用滴定法确定CO2的物质的量将样品配制成100mL溶液,从中取出20.00mL,用c mol•L-1的盐酸滴定(甲基橙作指示剂).当溶液由黄色变为橙色,且保持30s不变时,停止滴定.平行测定三次,有关实验数据记录如下表.m1 g样品产生CO2的物质的量为0.125cmol.
| 实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.00 | 25.02 |
| 2 | 20.00 | 0.20 | 28.80 |
| 3 | 20.00 | 1.30 | 26.28 |
①为了减小实验误差,量气管中加入的液体X为饱和碳酸氢钠溶液;
②若该装置气密性良好,读数平视,但测得的“CO2体积”数据仍然偏小,其原因可能是水准管的液面高于量气管中的液面.
(6)确定CO2的相对分子质量,选用甲、乙(限用“甲”、“乙”、“丙”进行填写)的实验数据为最佳.
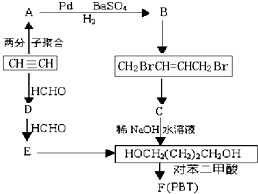 请根据以下知识解答
请根据以下知识解答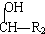 (R代表烃基,下同.)
(R代表烃基,下同.)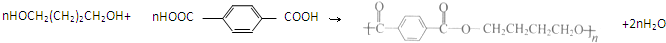 .
.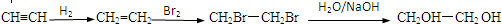 .
.