题目内容
下列图示实验合理的是( )
A、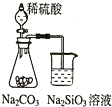 证明非金属性强弱:S>C>Si |
B、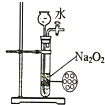 制备少量氧气 |
C、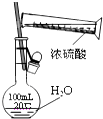 配制一定浓度硫酸溶液 |
D、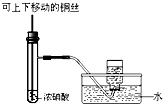 制备并收集少量NO2气体 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.发生强酸制取弱酸的反应,且均为最高价含氧酸;
B.过氧化钠为粉末状固体;
C.不能在容量瓶中稀释浓硫酸;
D.二氧化氮与水反应.
B.过氧化钠为粉末状固体;
C.不能在容量瓶中稀释浓硫酸;
D.二氧化氮与水反应.
解答:
解:A.硫酸与碳酸钠反应生成二氧化碳,二氧化碳与硅酸钠反应生成硅酸,则酸性为硫酸>碳酸>硅酸,所以非金属性S>C>Si,故A正确;
B.过氧化钠为粉末状固体,图中隔板不能使反应随时停止来制备少量氧气,故B错误;
C.不能在容量瓶中稀释浓硫酸,应在烧杯中稀释、冷却后转移到容量瓶中,故C错误;
D.二氧化氮与水反应,不能利用排水法收集,故D错误;
故选A.
B.过氧化钠为粉末状固体,图中隔板不能使反应随时停止来制备少量氧气,故B错误;
C.不能在容量瓶中稀释浓硫酸,应在烧杯中稀释、冷却后转移到容量瓶中,故C错误;
D.二氧化氮与水反应,不能利用排水法收集,故D错误;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,涉及酸性与非金属性比较、氧气的制备、二氧化氮的制备及收集、溶液配制等,把握化学反应原理及实验装置中的反应为解答的关键,注意实验操作的可行性、评价性分析,题目难度不大.

练习册系列答案
相关题目
下列关于实验原理或操作的叙述中,不正确的是( )

| A、用甲苯萃取溴水中的溴时,将溴的甲苯溶液从分液漏斗的上口倒出 |
| B、纸层析法主要是利用毛细现象和相似相溶原理进行物质分离 |
| C、许多金属或它们的混合物在火焰上灼烧时都会呈现特征焰色,可以检验金属或金属离子的存在,属于物理方法 |
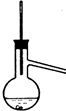
| D、利用如图装置进行蒸馏,会导致收集到的产品中混有高沸点杂质 |
火腿中加入亚硝酸钠,可使肉类长时间保持鲜红色,其原因是( )
| A、亚硝酸钠是防腐剂,可抑制细菌生长 |
| B、亚硝酸钠本身为鲜红色,覆盖在肉类表面 |
| C、亚硝酸钠跟肉类中的蛋白质反应 |
| D、亚硝酸钠跟氧气反应,抑制了肉类的氧化 |
已知:
锂离子电池的总反应为:LixC+Li1-xCoO2
C+LiCoO2;
锂硫电池的总反应为:2Li+S
Li2S
有关上述两种电池说法正确的是( )
锂离子电池的总反应为:LixC+Li1-xCoO2
| 放电 |
| 充电 |
锂硫电池的总反应为:2Li+S
| 放电 |
| 充电 |
有关上述两种电池说法正确的是( )
| A、锂离子电池放电时,Li+向负极迁移 |
| B、锂硫电池充电时,锂电极发生还原反应 |
| C、理论上两种电池的比能量相同 |
D、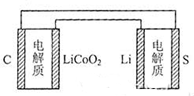 图中表示用锂离子电池给锂硫电池充电 图中表示用锂离子电池给锂硫电池充电 |
下列化学式表示的物质具有同分异构体的是( )
| A、CH2Cl2 |
| B、C2H5Cl |
| C、C2H4Br2 |
| D、CF2Cl2 |
根据下表信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径 | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A、氢化物的稳定性为H2T<H2R |
| B、氢氧化物碱性:L(OH)2<Q(OH)2 |
| C、L2+与R2-的核外电子数相等 |
| D、M与T形成的化合物具有两性 |
下列图示实验正确的是( )
A、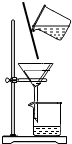 除去粗盐溶液中不溶物 |
B、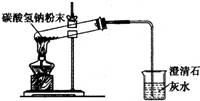 碳酸氢钠受热分解 |
C、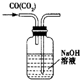 除去C0气体中的C02气体 |
D、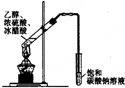 乙酸乙酯的制备演示实验 |
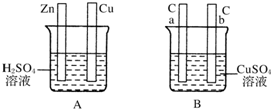 对如图中电极加以必要的连接并填空:
对如图中电极加以必要的连接并填空: