题目内容
4.从FeCl3溶液中得到FeCl3•6H2O固体操作作为在HCl气氛中加热,蒸发结晶.对(判断对错)分析 FeCl3+3H2O?Fe(OH)3+3HCl,直接加热,促进水解,生成的HCl易挥发,蒸发不能得到FeCl3•6H2O,以此来解答.
解答 解:FeCl3+3H2O?Fe(OH)3+3HCl,直接加热,促进水解,生成的HCl易挥发,蒸发不能得到FeCl3•6H2O,为抑制铁离子的水解,则从FeCl3溶液中得到FeCl3•6H2O固体操作作为在HCl气氛中加热,蒸发结晶,说法对,
故答案为:对.
点评 本题考查盐类水解原理的应用,为高频考点,把握铁离子水解生成的盐酸易挥发为解答的关键,侧重分析与应用能力的考查,注意水解的抑制作用,题目难度不大.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
14.下列反应不属于氧化反应的是( )
| A. | 乙醇在铜做催化剂、加热条件下与氧气反应生成乙醛 | |
| B. | 乙烯、乙醇分别使酸性高锰酸钾溶液褪色 | |
| C. | 苯在浓硫酸做催化剂、加热条件下与浓硝酸反应 | |
| D. | 甲烷在空气中燃烧 |
15.在水溶液中能大量共存的一组是( )
| A. | Cu2+、Na+、SO42-、Cl- | B. | Al3+、Na+、OH-、NO3- | ||
| C. | OH-、HCO3-、Ca2+、Na+ | D. | Mg2+、Na+、OH-、NO3- |
19.下列各组反应(表中物质均为反应物)中.反应刚开始时,放出氢气的速率最快的是( )
| 编号 | 金属(块状) | 酸的浓度及体积 | 反应温度(℃) |
| A | Mg0.1mol | 6mol/L硝酸10mL | 70 |
| B | Mg0.2mol | 3mol/L盐酸40mL | 60 |
| C | Fe0.2mol | 3mol/L盐酸50mL | 60 |
| D | Mg0.1mol | 3mol/L硫酸10mL | 60 |
| A. | A | B. | B | C. | C | D. | D |
5.NA表示阿伏加德罗常数,下列说法中不正确的是( )
| A. | 46g NO2和N2O4的混合气体中含有的原子个数为3NA | |
| B. | 常温下,4 g CH4含有NA个C-H共价键 | |
| C. | 10 mL质量分数为98%的H2SO4,加水至100 mL,H2SO4的质量分数为9.8% | |
| D. | 25℃时,pH=12的1.0 LNaClO溶液中水电离出的OH-的数目为0.01NA |
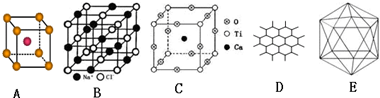



 有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料.D与A位于同一主族,是构成地球上矿物质的主要元素.请回答下列问题:
有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料.D与A位于同一主族,是构成地球上矿物质的主要元素.请回答下列问题: