题目内容
如图是电解精炼铜装置,其中c、d为铜电极.则下列有关的判断不正确的是( )


| A、c为粗铜板、d为纯铜板 |
| B、电解过程中,SO42-浓度几乎不变 |
| C、电解过程中,阳极质量的减少与阴极质量的增加相等 |
| D、电解过程中,c电极板附近沉积不溶物,d电极板质量增加 |
考点:原电池和电解池的工作原理
专题:
分析:根据电流方向知,c是阳极、d是阴极、a是正极、b是负极,c、d是铜板,则c电极上电极反应式为Cu-2e-=Cu 2+、d电极反应式为Cu2++2e-=Cu,电解精炼时粗铜作阳极、纯铜作阴极,据此分析解答.
解答:
解:A.c为阳极其电极材料是粗铜、d为阴极其电极材料是纯铜,故A正确;
B.电解过程中,硫酸根离子不参加反应,溶液体积几乎不变,所以硫酸根离子浓度几乎不变,故B正确;
C.电解过程中,阳极上不仅有铜还有其它金属失电子,阴极上只有铜离子得电子,所以阳极减少的质量不等于阴极增加的质量,故C错误;
D.电解过程中,c电极上部分不活泼金属以固体单质形式进入溶液,形成阳极泥,d电极上铜离子析出,所以质量增加,故D正确;
故选C.
B.电解过程中,硫酸根离子不参加反应,溶液体积几乎不变,所以硫酸根离子浓度几乎不变,故B正确;
C.电解过程中,阳极上不仅有铜还有其它金属失电子,阴极上只有铜离子得电子,所以阳极减少的质量不等于阴极增加的质量,故C错误;
D.电解过程中,c电极上部分不活泼金属以固体单质形式进入溶液,形成阳极泥,d电极上铜离子析出,所以质量增加,故D正确;
故选C.
点评:本题考查电解原理,明确阴阳极上发生的反应是解本题关键,注意:阳极是活泼金属时,阳极上金属失电子而不是溶液中阴离子失电子,为易错点.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
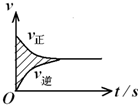 在容积固定的2L 密闭容器中进行着一个可逆反应X(g)+2Y(g)?2Z(g),用Y的物质的量浓度改变表示的反应速率v正、v逆与时间的关系如图所示.已知v的单位为mol?(L?s)-1,则图中阴影部分的面积表示( )
在容积固定的2L 密闭容器中进行着一个可逆反应X(g)+2Y(g)?2Z(g),用Y的物质的量浓度改变表示的反应速率v正、v逆与时间的关系如图所示.已知v的单位为mol?(L?s)-1,则图中阴影部分的面积表示( )| A、X的物质的量浓度的减少 |
| B、Y的物质的量浓度的减少 |
| C、Z的物质的量的增加 |
| D、Y的物质的量的减少 |
下列化学方程式不能用Ba2++SO42-═BaSO4↓来表示的是( )
| A、Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 |
| B、BaCO3+H2SO4═BaSO4↓+CO2↑+H2O |
| C、Na2SO4+BaCl2═BaSO4↓+2NaCl |
| D、BaCl2+H2SO4═BaSO4↓+2HCl |
下列反应既属于化合反应,又属于氧化还原反应的是( )
| A、Fe+2HCl═H2+FeCl2 |
| B、2FeCl2+Cl2═2FeCl3 |
| C、CaO+H2O═Ca(OH)2 |
| D、2Fe(OH)3═Fe2O3+3H2O |
若agCO2含b个分子,则阿伏加德罗常数的值为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
已知H2(g)、CO(g)、CH3OH(l)的燃烧热△H分别是-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.下列有关叙述正确的是( )
| A、甲醇不完全燃烧生成CO和液态水的热化学方程式:CH3OH(l)+O2 (g)═CO(g)+2H2O(l)△H1=-1009.5kJ?mol-1 |
| B、已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 |
| C、2H2O(g)═2H2(g)+O2(g)△H1=+571.6 kJ?mol-1 |
| D、△H>0的化学反应在高温条件下才能自发进行 |