题目内容
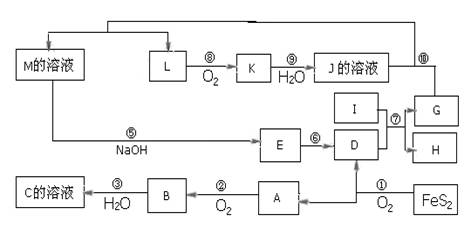
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出),大部分反应在工业生产中得到实际应用。已知Ⅰ、G是单质,且Ⅰ是一种既能与酸反应又能与碱反应生成氢气的金属,L是一种无色气体,K是一种红棕色气体,E是一种红褐色沉淀。
请填写下列空白:
(1)写出下列物质的化学式:C: ;J: 。
(2)写出下列反应的化学反应方程式:
反应⑦: 。
反应⑩: 。
(3)写工业上NH3与O2在一定条件下制取L的化学方程式: 。

请填写下列空白:
(1)写出下列物质的化学式:C: ;J: 。
(2)写出下列反应的化学反应方程式:
反应⑦: 。
反应⑩: 。
(3)写工业上NH3与O2在一定条件下制取L的化学方程式: 。
(每空2分,共10分,条件未写扣一分)
(1)C:H2SO4 J: HNO3
(2)反应⑦ : Fe2O3 + 2Al Al2O3 + 2Fe
Al2O3 + 2Fe
反应⑩:Fe + 4HNO3 = Fe(NO3)3 +NO↑ +2 H2O
(3)4NH3 + 5O2 4NO + 6H2O
4NO + 6H2O
(1)C:H2SO4 J: HNO3
(2)反应⑦ : Fe2O3 + 2Al
 Al2O3 + 2Fe
Al2O3 + 2Fe反应⑩:Fe + 4HNO3 = Fe(NO3)3 +NO↑ +2 H2O
(3)4NH3 + 5O2
 4NO + 6H2O
4NO + 6H2O试题分析:I是既能与强酸反应生成氢气又能与强碱反应生成氢气的金属,判断为Al,K是一种红棕色气体,判断为NO2;D的俗名叫铁红为Fe2O3;,A是形成酸雨的主要气体为SO2,由反应4FeS2+11O2
 2Fe2O3+8SO2知A、D为Fe2O3、A为SO2,结合A+O2 →B知,A为SO2,D为Fe2O3,B为SO3,C为H2SO4;I是既能与强酸反应生成氢气又能与强碱反应生成氢气的金属为Al;G、H为Al2O3和Fe中的一种;由K是一种红棕色气体,K为NO2,J为HNO3,L为NO;又由G+HNO3 →M+NO↑分析知G为Fe,H为Al2O3;M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2;F为Fe(NO3)3或Fe2(SO4)3;E应为Fe(OH)3,至此全部物质已确定,分别为:A、SO2;B、SO3;C、H2SO4;D、Fe2O3;E、Fe(OH)3;F、Fe(NO3)3或Fe2(SO4)3;G、Fe;H、Al2O3;I、Al;J、HNO3;K、NO2;L、NO;M、Fe(NO3)2;题目所涉及的问题可顺利解决。
2Fe2O3+8SO2知A、D为Fe2O3、A为SO2,结合A+O2 →B知,A为SO2,D为Fe2O3,B为SO3,C为H2SO4;I是既能与强酸反应生成氢气又能与强碱反应生成氢气的金属为Al;G、H为Al2O3和Fe中的一种;由K是一种红棕色气体,K为NO2,J为HNO3,L为NO;又由G+HNO3 →M+NO↑分析知G为Fe,H为Al2O3;M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2;F为Fe(NO3)3或Fe2(SO4)3;E应为Fe(OH)3,至此全部物质已确定,分别为:A、SO2;B、SO3;C、H2SO4;D、Fe2O3;E、Fe(OH)3;F、Fe(NO3)3或Fe2(SO4)3;G、Fe;H、Al2O3;I、Al;J、HNO3;K、NO2;L、NO;M、Fe(NO3)2;题目所涉及的问题可顺利解决。(1)依据题干条件和推断,A是酸雨主要成分为:SO2,A+O2→B,B+H2O→C,推知C为H2SO4;D为铁红Fe2O3,E为Fe(OH)3,J为HNO3。
(2)反应⑦的化学方程式为铝热反应,化学方程式为:Fe2O3+2Al
 Al2O3+2Fe。
Al2O3+2Fe。反应⑩的方程式为:Fe + 4HNO3 = Fe(NO3)3 +NO↑ +2 H2O。
(3)根据教材知识书写其方程式为4NH3 + 5O2
 4NO + 6H2O。
4NO + 6H2O。点评:本题考查了无机化合物的性质转化关系和性质应用,主要利用特征现象进行分析推断各物质,抓住题眼①和题干信息,结合反应和转化关系判断出各物质是解题关键。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目

 乙
乙 丙
丙 甲
甲