题目内容
乙酸与含
O的乙醇反应,反应后混合物中含
O的物质有( )
18 8 |
18 8 |
| A、乙醇 | B、乙酸、乙酸乙酯 |
| C、乙酸乙酯、乙醇 | D、水 |
考点:聚合反应与酯化反应
专题:有机反应
分析:酯化反应原理是酸脱羟基醇脱氢,据此解题.
解答:
解:酯化反应原理是酸脱羟基醇脱氢,醇中的氧原子可进入酯,且酯化反应为可逆反应,则混合物中含
O的物质为乙酸乙酯、乙醇,故选C.
18 8 |
点评:本题考查酯化反应的原理,难度不大,注意酯化反应原理是酸脱羟基醇脱氢.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案
相关题目
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、常温下,0.1L 1mol?L-1的醋酸电离出H+的物质的量为0.1mol |
| B、含1 mol HCl的盐酸与足量Fe反应,Fe所失去的电子总数为2NA |
| C、常温常压下,32 g O2和32 g O3所含氧原子数都是2NA |
| D、标准状况下,11.2 L H2O含有0.5NA个分子 |
下列表示对应化学反应的离子方程式正确的是( )
| A、NaHCO3溶液与醋酸溶液反应:HCO3-+H+═CO2↑+H2O | ||||
| B、氯化铝溶液与过量氨水反应:Al3++4OH-═AlO2-+2H2O | ||||
| C、Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | ||||
D、NaOH溶液与氯化铵溶液在加热下反应:NH4++OH-
|
聚合物 的单体是( )
的单体是( )
 的单体是( )
的单体是( )A、 |
B、 |
C、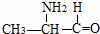 |
D、 |
某溶液中存在大量的H+、Cl-,该溶液中还可能大量存在的离子是( )
| A、HCO3- |
| B、OH- |
| C、Al3+ |
| D、Ag+ |
用NA表示阿伏加德罗常数的值.下列叙述中一定正确的是( )
| A、一定条件下某密闭容器盛有0.1mol N2和0.3mol H2,充分反应后转移电子数为0.6NA |
| B、50mL 18.4mol?L-1浓硫酸与足量铜加热反应,生成SO2的分子数为0.46NA |
| C、一定条件下4.6g Na完全与O2反应生成7.2g产物,失去的电子数为0.2NA |
| D、电解1L NaCl溶液至c(OH-)=0.2mol?L-1,转移电子数为0.4NA(假设电解过程中溶液体积不变) |
