题目内容
12.某溶液含有①NO3-②HCO3-③SO32-④CO32-⑤SO42-等五种阴离子.向其中加入少量的Na2O2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积的变化)( )| A. | ① | B. | ①②④ | C. | ①③⑤ | D. | ①③④⑤ |
分析 Na2O2与水反应生成氢氧化钠,溶液呈碱性,Na2O2具有强氧化性,能与OH-反应的离子和具有还原性的离子的浓度会发生改变.同时溶液中存在反应生成的离子,该离子浓度也会变化.
解答 解:Na2O2与水反应生成氢氧化钠,溶液呈碱性,HCO3-与OH-反应生成CO32-,则HCO3-离子浓度减小,CO32-离子浓度增大;
Na2O2具有强氧化性,将SO32-氧化为SO42-,则SO32-离子浓度减小,SO42-浓度增大;
NO3-浓度基本不变.
故选A.
点评 本题考查Na2O2的性质以及离子反应,难度不大,注意Na2O2的强氧化性.

练习册系列答案
相关题目
2.实验室有一包白色固体,可能含有Na2CO3、NaHCO3和NaCl中的一种或多种.下列根据实验事实得出的结论正确的是( )
| A. | 取一定量固体,溶解,向溶液中滴加适量AgNO3溶液,观察到有白色沉淀生成,说明原固体中一定含有NaCl | |
| B. | 取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成,说明原固体中一定含有Na2CO3 | |
| C. | 取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一定含有Na2CO3 | |
| D. | 称取3.80g固体,加热至恒重,质量减少了0.620g.用足量稀盐酸溶解残留固体,充分反应后,收集到0.880g气体,说明原固体中仅含有Na2CO3和NaHCO3 |
20.同温、同压下,相同体积的下列气体中质量最大的是( )
| A. | 二氧化碳 | B. | 甲烷 | C. | 氧气 | D. | 氯化氢 |
7.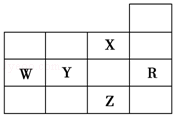 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A. | W元素的电负性大于Y元素的电负性 | |
| B. | X元素是电负性最大的元素 | |
| C. | p能级未成对电子最多的是Z元素 | |
| D. | Y、Z的阴离子电子层结构都与R原子的相同 |
4.下列物质属于盐的是( )
| A. | 氧化钙 | B. | 氯化铁 | C. | 氯化氢 | D. | 氢氧化钠 |
8.欲将CaCl2溶液中含有的盐酸除掉,应采用的最好方法是( )
| A. | 加生石灰,过滤 | B. | 加适量的AgNO3溶液 | ||
| C. | 加过量的Na2CO3溶液 | D. | 加CaCO3粉末,过滤 |