题目内容
10.下列说法正确的是( )| A. | 同温同压下,相同体积气体所含原子个数相同 | |
| B. | 标准状况下1摩尔H2SO4的体积约为22.4 L | |
| C. | 同温同压下,相同体积的H2、O2,其质量比为1:16 | |
| D. | 1摩尔的气体只有在标准状况下才能是22.4 L |
分析 A.同温同压下相同体积的气体具有相同的物质的量,不一定具有相同原子数;
B.标准状况下,硫酸的状态不是气体;
C.同温同压下,相同体积的气体具有相同物质的量,然后根据m=nM计算二者质量之比;
D.温度和压强都影响气体体积,不是在标准状况下,气体摩尔体积也可能为22.4L/mol.
解答 解:A.气体分子中含有原子数不一定相等,则同温同压下,相同体积气体所含原子个数不一定相同,故A错误;
B.标准状况下,硫酸不是气体,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.同温同压下,相同体积的H2、O2具有相同的物质的量,则其质量比=摩尔质量成正比=2g/mol:32g/mol=1:16,故C正确;
D.由于温度和压强影响气体体积,则1摩尔的气体不在标准状况下也可能是22.4 L,故D错误;
故选C.
点评 本题考查了物质的量的计算、阿伏伽德罗定律及推论,题目难度中等,明确物质的量与摩尔质量、气体摩尔体积的关系为解答关键,B为易错点,注意标准状况下气体摩尔体积的使用条件.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
5.将amL的乙炔气体,通入盛有bg苯的试管中.则所得混合物中碳的质量分数为( )
| A. | $\frac{12}{13}$ | B. | $\frac{1}{7}$ | C. | $\frac{6}{7}$ | D. | 无法确定 |
1.用如图装置能达到有关实验目的是( )
| A. |  电解精炼铝 | B. | 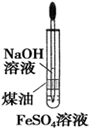 制备Fe(OH)3 | ||
| C. | 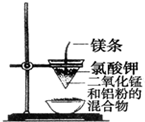 可制得金属锰 | D. | 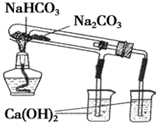 验证NaHCO3和Na2CO3的热稳定性 |
5.经催化加氢后,不能得到2-甲基戊烷的是( )
| A. | CH3CH═CHCH(CH3)2 | B. | (CH3)2C═CHCH2CH3 | ||
| C. | CH3CH═C(CH3)CH2CH3 | D. | CH2═CH CH2CH(CH3)2 |
15.一定条件下,下列各组物质中,Y既能与X反应又能与Z反应的有几组( )
| 序号 | X | Y | Z |
| ① | NaHSO4溶液 | Al(OH)3 | 稀硫酸 |
| ② | CaCl2溶液 | SO2 | CaSO3 |
| ③ | HF溶液 | Si | Ba(OH)2 |
| ④ | Fe Cl3溶液 | Fe | 浓硝酸 |
| A. | 1组 | B. | 2组 | C. | 3组 | D. | 4组 |
2.下列关于有机物的说法正确的是( )
| A. | 乙烯、甲苯、甲烷分子中的所有原子都在同一平面上 | |
| B. | 除去乙烷中的乙烯时,通入氢气并加催化剂加热 | |
| C. | C3H8的二氯代物共有3种 | |
| D. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
20.下列气态氢化物中,按稳定性由强到弱的顺序排列的是( )
| A. | HI、HBr、HCl、HF | B. | HCl、H2S、PH3、SiH4 | ||
| C. | H2O、H2S、HCl、HBr | D. | H2O、HF、NH3、CH4 |