题目内容
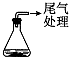
 如图所示,水槽中试管内有一枚铁钉,放置数天观察:
如图所示,水槽中试管内有一枚铁钉,放置数天观察:(1)铁钉在逐渐生锈,则铁钉的腐蚀属于
(2)若试管内液面上升,则原溶液是
电极反应:负极:
(3)若试管内液面下降,则原溶液是
(4)若溶液甲为水,溶液乙为海水,则铁钉在
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:(1)铁在潮湿的空气中易发生电化学腐蚀;
(2)中性条件下,铁发生吸氧腐蚀,负极上铁失电子,正极上氧气得电子;
(3)酸性条件下,铁发生析氢腐蚀,负极上铁失电子,正极上氢离子得电子;
(4)海水中存在电解质溶液,铁易发生电化学腐蚀.
(2)中性条件下,铁发生吸氧腐蚀,负极上铁失电子,正极上氧气得电子;
(3)酸性条件下,铁发生析氢腐蚀,负极上铁失电子,正极上氢离子得电子;
(4)海水中存在电解质溶液,铁易发生电化学腐蚀.
解答:
解:(1)铁在潮湿的空气中易发生电化学腐蚀,所以水槽中试管内有一枚铁钉,铁钉在逐渐生锈,则铁钉的腐蚀属于电化学腐蚀;
故答案为:电化学;
(2)中性条件下,铁发生吸氧腐蚀,负极上铁失电子,负极的电极反应为:Fe-2e-=Fe2+,正极上氧气得电子生成氢氧根离子,则其电极反应为:2H2O+O2+4e-=4OH-;
故答案为:中;吸氧;Fe-2e-=Fe2+;2H2O+O2+4e-=4OH-;
(3)若试管内液面下降,说明气体的体积增大,酸性条件下,铁发生析氢腐蚀,负极上铁失电子,负极的反应式为:Fe-2e-=Fe2+,正极上氢离子得电子生成氢气,其反应的方程式为:2H++2e-=H2↑;
故答案为:酸;析氢;Fe-2e-=Fe2+;2H++2e-=H2↑;
(4)海水中存在电解质溶液,铁易发生电化学腐蚀,所以铁钉在乙中的腐蚀的速度快,故答案为:乙.
故答案为:电化学;
(2)中性条件下,铁发生吸氧腐蚀,负极上铁失电子,负极的电极反应为:Fe-2e-=Fe2+,正极上氧气得电子生成氢氧根离子,则其电极反应为:2H2O+O2+4e-=4OH-;
故答案为:中;吸氧;Fe-2e-=Fe2+;2H2O+O2+4e-=4OH-;
(3)若试管内液面下降,说明气体的体积增大,酸性条件下,铁发生析氢腐蚀,负极上铁失电子,负极的反应式为:Fe-2e-=Fe2+,正极上氢离子得电子生成氢气,其反应的方程式为:2H++2e-=H2↑;
故答案为:酸;析氢;Fe-2e-=Fe2+;2H++2e-=H2↑;
(4)海水中存在电解质溶液,铁易发生电化学腐蚀,所以铁钉在乙中的腐蚀的速度快,故答案为:乙.
点评:本题考查了钢铁的电化学腐蚀,注意酸性条件下,钢铁发生析氢腐蚀,弱酸性或中性条件下,钢铁发生吸氧腐蚀,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
生活中常用的塑料及橡胶制品都属于( )
| A、传统非金属无机材料 |
| B、新型非金属无机材料 |
| C、高分子材料 |
| D、复合材料 |