题目内容
(14分 )A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,B的产量是衡量一个国家石油化工发展水平的标志,他们之间并能进行如图所示的相互转化。

(1)写出A的结构简式 ,F中所含决定化学性质的原子团的名称为
(2)下列反应的化学方程式并注明反应类型
反应①: ,反应类型
反应②: ,反应类型
反应③: ,反应类型
反应④: ,反应类型
(14分)(1)C2H5OH 或 CH3CH2OH 羧基
(2)①2CH3CH2OH + 2Na →2CH3CH2ONa + H2↑ 取代反应
②CH2=CH2+H2O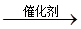 CH3CH2OH,加成反应
CH3CH2OH,加成反应
③CH3COOH + CH3CH2OH CH3COOCH2CH3
+ H2O 酯化反应或取代反应
CH3COOCH2CH3
+ H2O 酯化反应或取代反应
④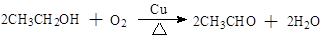 ,氧化反应
,氧化反应
【解析】B的产量是衡量一个国家石油化工发展水平的标志,则B是乙烯。乙烯含有碳碳双键,能和水发生加成反应,生成乙醇,A是乙醇。乙醇含有羟基,能和钠反应生成氢气和乙醇钠。也能和乙酸发生酯化反应生成乙酸乙酯,即C是乙酸乙酯,乙酸乙酯水解即生成乙酸。乙醇能发生催化氧化生成乙醛,即D是乙醛,乙醛再氧化生成乙酸,即F是乙酸,含有的官能团是羧基。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案(本题14分)某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中加入l—2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe、Br2谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性:Fe>Br2,故上述实验现象不是发生化学反应所致,则溶液里黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Fe<Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(3)设计实验并验证
丙同学为验证乙同学的观点。选用下列某些试剂设计两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a、酚酞试液 b、四氯化碳 c、无水酒精 d、硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
|
| 选用试剂(填序号) | 实验现象 |
| 方案1 |
|
|
| 方案2 |
|
|
(4)结论
氧化性:Fe<Br2,在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(5)实验后的思考
在2molFeBr2溶液中通入一定量的Cl2,当有33.6L Cl2(标准状况)与FeBr2溶液发生了反应,所发生反应的离子反应方程式为 。
(14分)下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:
| a | | | |||||
| | | | b | c | d | | |
| e | | f | | | g | | |
(2) e 与f两元素最高价氧化物的水化物相互反应的化学方程式为
_________________________________________________
(3)e在空气中燃烧的产物所含化学键的类型为__________、__________。
(4) 化合物ca3的电子式为 ,c和d两种元素氢化物的稳定性更强的是 _______(填物质的化学式)。
