题目内容
下列变化中,需要加入氧化剂的是( )
A.SO2→SO3 B.HCl→H2 C.FeCl2→FeCl3 D.Fe2O3→Fe
AC
【解析】
试题分析:A.在 SO2→SO3中S的化合价升高,失去电子,所以要加入氧化剂,正确;B. 在HCl→H2中H的化合价降低,得到电子,所以要加入还原剂,错误;C. 在FeCl2→FeCl3中Fe的化合价升高,失去电子,所以要加入氧化剂,正确;D. 在Fe2O3→Fe中Fe的化合价降低,得到电子,所以要加入还原剂,错误。
考点:考查氧化还原反应中元素的化合价的升降与电子转移、物质的作用的关系的知识。

(16分)A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
阳离子 | Na+、Al3+、Ba2+、NH4+ |
阴离子 | Cl-、OH-、CO32-、SO42- |
分别取四种物质进行实验,实验结果如下:
①A、D溶液呈碱性,B呈酸性,C呈中性
②A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失
③A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试纸变蓝
回答下列问题:
(1)A的化学式是_________,用电子式表示C的形成过程:________________ 。
(2)向A溶液中通入适量CO2,使生成的沉淀恰好溶解,所得溶液中各离子物质的量浓度由大到小的顺序是:________________________ 。
(3)写出③的离子方程式_______________________________________________ 。
(4)简述D溶液呈碱性的理由___________________________________________ 。
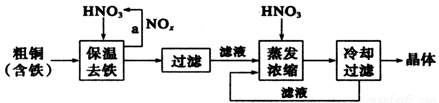

 OH—+H3O+, 则液态NH3电离的方程式是 ,液态N2O4电离得到电子数相差18的阴阳离子,因此可用Cu与液态N2O4反应制备无水硝酸铜,其反应的化学方程式是 。
OH—+H3O+, 则液态NH3电离的方程式是 ,液态N2O4电离得到电子数相差18的阴阳离子,因此可用Cu与液态N2O4反应制备无水硝酸铜,其反应的化学方程式是 。 BCl3空间形状为 (用文字描述)。
BCl3空间形状为 (用文字描述)。 键数目为 。
键数目为 。