题目内容
11.在通常条件下,下列各组物质的性质排列正确的是( )| A. | Na、Mg、Al 的第一电离能逐渐增大 | B. | O、F、N 的电负性逐渐增大 | ||
| C. | S2-、Cl-、K+的半径逐渐增大 | D. | 热稳定性:HF>H2O>NH3 |
分析 A.Mg最外层为全充满结构,难以失去电子;
B.同周期元素从左到右,电负性逐渐增强;
C.核外电子排布相同的离子,核电荷数越大离子半径越小;
D.元素的非金属性越强,对应的氢化物越稳定.
解答 解:A.Mg的最外层为3s电子全满,稳定结构,难以失去电子,第一电离能最大,Na的最小,故A错误;
B.同周期元素从左到右,电负性逐渐增强,电负性F>O>N,故B错误;
C.核外电子排布相同的离子,核电荷数越大离子半径越小,应为S2->Cl->K+,故C错误;
D.非金属性F>O>N,元素的非金属性越强,对应的氢化物越稳定,故D正确.
故选D.
点评 本题考查了原子结构与元素周期律的关系,题目难度不大,明确元素周期律内容为解答关键,A为易错点,注意ⅡA族、ⅤA族元素的电负性反常,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
19.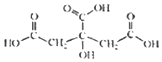 柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )
柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )
 柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )
柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )| A. | 柠檬酸的分子式是C6H8O7 | |
| B. | 柠檬酸是易溶于水的有机物 | |
| C. | 1mol柠檬酸足量的钠反应生成2.0mol的氢气 | |
| D. | 柠檬酸只能发生取代反应 |
2. 已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( )
已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( )
 已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( )
已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( )| A. | 由图甲知,A点SO2的平衡浓度为0.4 mol/L | |
| B. | 由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2 | |
| C. | 达平衡后,缩小容器容积,v正和v逆都增大 | |
| D. | 增大SO2浓度,v正增大v逆减小 |
6.“玉兔”号月球车用${\;}_{94}^{238}$Pu作为热源材料.下列关于${\;}_{94}^{238}$Pu的说法正确的是( )
| A. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U互为同位素 | |
| B. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu互为同素异形体 | |
| C. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu具有相同的最外层电子数 | |
| D. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U具有完全相同的化学性质 |
16.下列说法正确的是( )
| A. | 铅蓄电池在充电过程中,阴极得到电子质量增加 | |
| B. | 1 mol羟基含电子数约为7×6.02×1023 | |
| C. | 0.1 mol•L-1 CH3COOH溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$的值减小 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
3.下列有关化学用语表示正确的是( )
| A. | 乙烯的比例模型: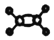 | B. | 四氯化碳的电子式: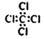 | ||
| C. | 苯酚的结构式: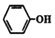 | D. | 乙醛的结构式:CH3CHO |
20.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的核外有7个电子,在周期表中Y位于ⅡA族,Y、Z原子的最外层电子数之和等于W原子的最外层电子数,W的氢化物热稳定性在同周期元素中最强.下列说法正确的是( )
| A. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| B. | 元素Y、W的简单离子具有相同的电子层结构 | |
| C. | Z的最高价氧化物对应水化物的酸性比X的强 | |
| D. | 由X与Y两种元素组成的简单化合物是离子化合物 |
1.用自来水养金鱼时,将水注入鱼缸以前需把水放在阳光下暴晒一段时间,目的是( )
| A. | 起到杀菌作用 | B. | 使水中次氯酸分解 | ||
| C. | 提高水的温度 | D. | 增加水中氧气的含量 |
