题目内容
1.为确定某溶液由以下离子Na+、Mg2+、Ba2+、SO42-、I-、CO32-中的哪几种微粒组成.进行以下实验,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象.为确定该溶液的组成,还需检验的离子是( )| A. | Na+ | B. | SO42- | C. | Ba2+ | D. | Mg2+ |
分析 ①用pH计测试,溶液显弱酸性,则一定含强酸根离子、弱碱离子,则一定含Mg2+;
②加氯水和淀粉无明显现象,则一定不含I-,再结合离子的共存来解答.
解答 解:②加氯水和淀粉无明显现象,则一定不含I-,
①用pH计测试,溶液显弱酸性,则一定含强酸根离子、弱碱离子,则一定含Mg2+、SO42-,则不含CO32-;
因SO42-、Ba2+不能共存,则不含Ba2+,
不能确定的离子为Na+,即还需要检验Na+,
故选A.
点评 本题考查常见离子的检验,为高频考点,把握实验中发生的反应及离子检验的方法、现象与结论的关系为解答的关键,侧重分析与实验能力的考查,注意离子的共存及盐类水解的应用,题目难度不大.

练习册系列答案
相关题目
11.已知16S和34Se位于同一主族,下列关系不正确的是( )
| A. | 热稳定性:H2Se>H2S | B. | 原子半径:Se>O | ||
| C. | 酸性:H2SO4>H2SeO4 | D. | 还原性:Se2->Cl- |
9.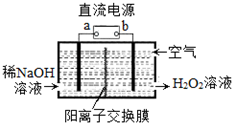 H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示,初始溶液为氢氧化钠溶液:下列说法正确的是( )
H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示,初始溶液为氢氧化钠溶液:下列说法正确的是( )
 H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示,初始溶液为氢氧化钠溶液:下列说法正确的是( )
H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示,初始溶液为氢氧化钠溶液:下列说法正确的是( )| A. | a为负极 | |
| B. | 通入空气的电极反应式为O2+2e-+2H+═H2O2 | |
| C. | 电解一段时间后,左侧溶液pH降低 | |
| D. | 若生成17g双氧水,则有1molH+从左侧向右侧迁移 |
16.化学与人们的生活关系密切,下列说法不正确的是( )
| A. | 氯气可用于自来水的杀菌消毒 | B. | 氧化铁可用于红色油漆和涂料 | ||
| C. | 油脂可用于在碱性溶液制取肥皂 | D. | 含氮、磷的污水可用于给土壤施肥 |
13.火药是中国古代四大发明之一,由硫磺、火硝和木炭粉均匀混合而成,点燃后可能发生的反应:S+2KNO3+3C═N2↑+3CO2↑+X(已配平),则物质X是( )
| A. | K2S | B. | SO2 | C. | H2S | D. | SO3 |
10.生石灰常用于治理酸性废水,下列说法合理的是( )
| A. | 生石灰主要成分是碱性化合物 | B. | 该过程只发生了物理变化 | ||
| C. | 生石灰主要成分是酸性化合物 | D. | 该过程同时实现了水软化 |
5.已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,则下列说法错误的是( )
| A. | Z的氢化物的沸点是同主族元素中最高的 | |
| B. | 由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒只有2种 | |
| C. | 仅由X、Y两种元素组成的化合物不止一种 | |
| D. | X和Z可以组成原子个数比分别为1:1和2:1常温下为液态的两种化合物 |
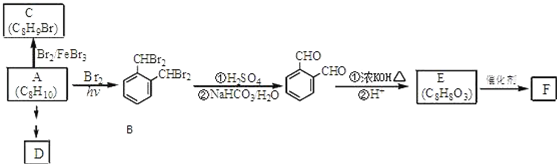
 ;
;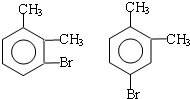 ;
;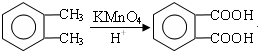 ;
; .(提示
.(提示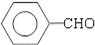 $\underset{\stackrel{①浓KOH、△}{→}}{②{H}^{+}}$
$\underset{\stackrel{①浓KOH、△}{→}}{②{H}^{+}}$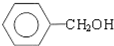 +
+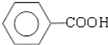 )
) .
.