题目内容
下列说法中错误的是( )
| A、若XY4分子中X原子处于正四面体的中心,则XY4分子为非极性分子 |
| B、C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 |
| C、在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
| D、短周期元素离子aXm+和bYn-具有相同的电子层结构,则a>b |
考点:极性分子和非极性分子,配合物的成键情况,氢键的存在对物质性质的影响
专题:化学键与晶体结构
分析:A、若XY4分子中X原子处于正四面体的中心,则正负电荷中心重合;
B、分子间存在氢键使物质的熔沸点异常的高;
C、[Cu(NH3)4]2+离子中,NH3给出孤对电子,Cu2+提供空轨道;
D、X失去电子后和Y得电子后具有相同的电子层结构,根据些分析.
B、分子间存在氢键使物质的熔沸点异常的高;
C、[Cu(NH3)4]2+离子中,NH3给出孤对电子,Cu2+提供空轨道;
D、X失去电子后和Y得电子后具有相同的电子层结构,根据些分析.
解答:
解:A、若XY4分子中X原子处于正四面体的中心,则正负电荷中心重合,所以XY4分子为非极性分子,故A正确;
B、分子间存在氢键使物质的熔沸点异常的高,而C2H5OH分子间存在氢键,所以C2H5OH的氟点比C2H5Br高,故B正确;
C、[Cu(NH3)4]2+离子中,NH3给出孤对电子,Cu2+提供空轨道,故C错误;
D、X失去电子后和Y得电子后具有相同的电子层结构,所以原子序数a>b,故D正确;
故选C.
B、分子间存在氢键使物质的熔沸点异常的高,而C2H5OH分子间存在氢键,所以C2H5OH的氟点比C2H5Br高,故B正确;
C、[Cu(NH3)4]2+离子中,NH3给出孤对电子,Cu2+提供空轨道,故C错误;
D、X失去电子后和Y得电子后具有相同的电子层结构,所以原子序数a>b,故D正确;
故选C.
点评:本题考查分子的极性、氢键、配位键和电子层结构,综合性强,但比较容易.

练习册系列答案
相关题目
下列说法正确的是( )
| A、含硅材料广泛用于太阳能电板、半导体材料、光纤通讯以及建筑材料等 |
| B、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| C、工艺师利用稀盐酸刻蚀石英制作艺术品 |
| D、粗硅制备单晶硅不涉及氧化还原反应 |
下列有关物质的性质比较,不正确的是( )
| A、熔点:Li>Cs |
| B、还原性:F->I- |
| C、热稳定性:H2O>H2S |
| D、酸性:H3PO4>H3AsO4 |
二维平面晶体所表示的化学式为AX2的是( )
A、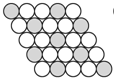 |
B、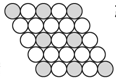 |
C、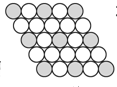 |
D、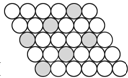 |
下列说法中正确的是( )
| A、H2SO4的摩尔质量是 98 g |
| B、1 mol H2O的质量是 18 g/mol |
| C、Cl-的摩尔质量是 35.5 g/mol |
| D、1 mol N2 的体积是 22.4 L |
