题目内容
19.下列离子方程式正确的是( )| A. | 金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | Cu与浓硝酸反应制 NO2:Cu+4HNO3(浓)═Cu2++2 NO3-+NO2↑+2H2O | |
| C. | 向同浓度的NaOH和Na2CO3,的混合液中加少量稀盐酸:CO32-+2H+═CO2↑+3H2O | |
| D. | 将 NaHSO4与 Ba(OH)2溶液混合至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
分析 A.电子、电荷不守恒;
B.硝酸完全电离;
C.加少量稀盐酸,只与NaOH反应;
D.中性时反应生成硫酸钡、硫酸钠和水.
解答 解:A.金属钠与水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.Cu与浓硝酸反应制 NO2的离子反应为Cu+4H++2NO3-═Cu2++2 NO2↑+2H2O,故B错误;
C.向同浓度的NaOH和Na2CO3的混合液中加少量稀盐酸的离子反应为OH-+H+═H2O,故C错误;
D.将 NaHSO4与 Ba(OH)2溶液混合至中性的离子反应为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
14.下列说法正确的是( )
| A. | KOH的摩尔质量是56 g | |
| B. | 一个碳原子的质量就是其相对原子质量 | |
| C. | 硫原子的质量就是硫的相对原子质量 | |
| D. | 氦气的摩尔质量以g•mol-1为单位时在数值上等于它的相对原子质量 |
8.设NA为阿伏加德罗常数的值.下列说法一定正确的是( )
| A. | 100mL1mol/L的盐酸中含HCl分子数为0.1NA | |
| B. | 7.8gNa2O2和Na2S的混合物中阴离子数目为0.2NA | |
| C. | 标准状况下,2.24L SO3中含有氧原子数目为0.3NA | |
| D. | 2gD216O中含中子、质子、电子数目均为NA |
15.某非金属元素在化学反应中从化合态变为游离态,则该元素( )
| A. | 一定被氧化 | B. | 一定被还原 | ||
| C. | 可能被氧化,也可能被还原 | D. | 化合价升高为O |
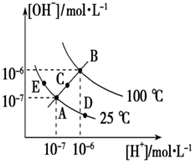 已知水的电离平衡曲线如图所示,试回答下列问题:
已知水的电离平衡曲线如图所示,试回答下列问题: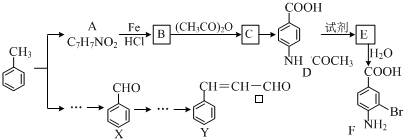
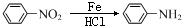
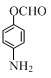
 +(CH3CO)2O→
+(CH3CO)2O→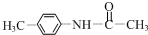 +CH3COOH.
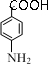
+CH3COOH.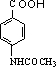 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$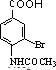 +HBr.
+HBr.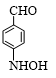 ;
;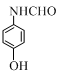 ;
; ;
;
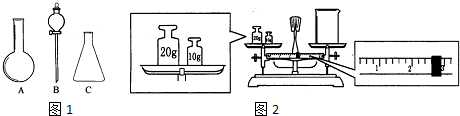

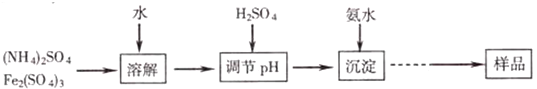
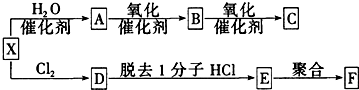
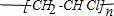 .
.