题目内容
在密闭容器中,反应X2(g)+2Y2(g)?2XY2(g)△H<0达到甲平衡,若只改变某一条件再达到乙平衡,则对此过程条件改变的分析正确的是( )
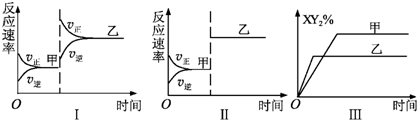

| A、图Ⅰ由甲至乙加入适当催化剂 |
| B、图Ⅱ由甲至乙扩大容器体积 |
| C、图Ⅲ由甲至乙增大压强 |
| D、图Ⅲ由甲至乙升高温度 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:反应X2(g)+2Y2(g)?2XY(g)△H<0,正反应为体积减小的放热的反应,
A.加催化剂正逆反应速率同等程度增大;
B.扩大体积,压强减小,正逆反应速率都降低,平衡向逆反应,逆反应速率降低较少;
C.增大压强,反应速率加快,到达平衡时间缩短,平衡向正反应方向移动,平衡时XY2的含量增大;
D.升高温度,应速率加快,到达平衡时间缩短,平衡向逆反应方向移动,平衡时XY2的含量减小.
A.加催化剂正逆反应速率同等程度增大;
B.扩大体积,压强减小,正逆反应速率都降低,平衡向逆反应,逆反应速率降低较少;
C.增大压强,反应速率加快,到达平衡时间缩短,平衡向正反应方向移动,平衡时XY2的含量增大;
D.升高温度,应速率加快,到达平衡时间缩短,平衡向逆反应方向移动,平衡时XY2的含量减小.
解答:
解:反应X2(g)+2Y2(g)?2XY(g)△H<0,正反应为体积减小的放热的反应,
A.加入催化剂,正、逆反应速率同等程度增大,平衡不移动,图象与实际不相符,故A错误;
B.扩大体积,压强减小,正逆反应速率都降低,平衡向逆反应,逆反应速率降低较少,图象中平衡不移动,图象与实际不相符,故B错误;
C.增大压强,反应速率加快,到达平衡时间缩短,平衡向正反应方向移动,平衡时XY2的含量增大,但图象中乙到达平衡时XY2的含量较小,与实际不符,故C错误;
D.升高温度,应速率加快,到达平衡时间缩短,平衡向逆反应方向移动,平衡时XY2的含量减小,图象与实际相符,故D正确,
故选D.
A.加入催化剂,正、逆反应速率同等程度增大,平衡不移动,图象与实际不相符,故A错误;
B.扩大体积,压强减小,正逆反应速率都降低,平衡向逆反应,逆反应速率降低较少,图象中平衡不移动,图象与实际不相符,故B错误;
C.增大压强,反应速率加快,到达平衡时间缩短,平衡向正反应方向移动,平衡时XY2的含量增大,但图象中乙到达平衡时XY2的含量较小,与实际不符,故C错误;
D.升高温度,应速率加快,到达平衡时间缩短,平衡向逆反应方向移动,平衡时XY2的含量减小,图象与实际相符,故D正确,
故选D.
点评:本题考查影响平衡和化学反应速率的因素,注意把握反应的特点及图象的分析为解答的关键,注意压强、温度对平衡的影响即可解答,题目难度不大.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、Na2CO3溶液的水解:CO32-+H3O+?HCO3-+H2O |
| B、AlCl3溶液中滴加浓氨水至过量:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| C、氯化亚铁溶液中加入硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
| D、向NaHSO4溶液中加入过量Ba(OH)2溶液:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
下列各组离子在水溶液中能大量共存的是( )
| A、Na+、NH4+、HCO3-、OH- |
| B、Fe3+、Zn2+、I-、SO42- |
| C、H+、K+、NO3-、SO42- |
| D、Ca2+、Na+、NO3-、CO32- |
用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A、1mol NH4+与1mol OH-所含的质子数均为10NA |
| B、标准状况下,22.4L CHCl3中含C-H键数目为NA |
| C、常温下,14g乙烯中含碳原子数为NA |
| D、常温下,pH=13的NaOH溶液中含OH-数目为NA |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、100 mL 1 mol?L-1的Na2CO3溶液中离子总数为0.3NA |
| B、若一筒120g的墨粉能打a个字,则平均每个字约含有10NA/a个碳原子 |
| C、在101kPa时,0.1NA个H2分子完全燃烧生成液态水,放出a kJ热量,表示氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=+20akJ?mol-1 |
| D、常温下28g14CO含有14 NA个电子 |
下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A、pH=4的0.1 mol?L-1的NaHC2O4溶液中:c(HC2O4-)>c (H2C2O4)>c(C2O42-) |
| B、0.1 mol?L-1的NaHCO3溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C、常温下,将醋酸钠、盐酸两溶液混合呈中性的溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
| D、常温下,等物质的量浓度的三种溶液:①(NH4)2SO4②NH4Cl ③(NH4)2Fe(SO4)2中c(NH4+):①<②<③ |
