题目内容
已知元素X、Y、Z、W的原子序数分别为6、8、11、13,请回答:
(1)写出下列元素符号Y W
(2)写出下列元素在周期表中的位置X W
(3)X和Y形成的稳定化合物的电子式为
(4)用电子式表示Z2Y的形成过程: .
(1)写出下列元素符号Y
(2)写出下列元素在周期表中的位置X
(3)X和Y形成的稳定化合物的电子式为
(4)用电子式表示Z2Y的形成过程:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:(1)元素X、Y、Z、W的原子序数分别为6、8、11、13,则X为C、Y为O、Z为Na、W为Al;
(2)周期数=电子层数,最外层电子数=族序数;
(3)X和Y形成的稳定化合物为CO2,分子中碳原子与氧原子之间形成2对共用电子对;
(4)Na2O属于离子化合物,由钠离子与氧离子构成,用Na原子、O原子电子式表示氧化钠形成.
(2)周期数=电子层数,最外层电子数=族序数;
(3)X和Y形成的稳定化合物为CO2,分子中碳原子与氧原子之间形成2对共用电子对;
(4)Na2O属于离子化合物,由钠离子与氧离子构成,用Na原子、O原子电子式表示氧化钠形成.
解答:
解:(1)元素X、Y、Z、W的原子序数分别为6、8、11、13,则X为C、Y为O、Z为Na、W为Al,
故答案为:O;Al;
(2)X为碳元素,原子结构示意图为 ,故处于第二周期ⅣA族;
,故处于第二周期ⅣA族;
W为Al元素,原子结构示意图为 ,故处于第三周期ⅢA族,
,故处于第三周期ⅢA族,
故答案为:第二周期ⅣA族;第三周期ⅢA族;
(3)X和Y形成的稳定化合物为CO2,分子中碳原子与氧原子之间形成2对共用电子对,其电子式为: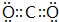 ,故答案为:
,故答案为: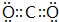 ;
;
(4)Na2O属于离子化合物,由钠离子与氧离子构成,用Na原子、O原子电子式表示氧化钠形成过程为: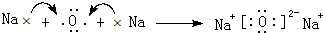 ,
,
故答案为: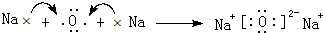 .
.
故答案为:O;Al;
(2)X为碳元素,原子结构示意图为
 ,故处于第二周期ⅣA族;
,故处于第二周期ⅣA族;W为Al元素,原子结构示意图为
 ,故处于第三周期ⅢA族,
,故处于第三周期ⅢA族,故答案为:第二周期ⅣA族;第三周期ⅢA族;
(3)X和Y形成的稳定化合物为CO2,分子中碳原子与氧原子之间形成2对共用电子对,其电子式为:
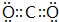 ,故答案为:
,故答案为: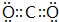 ;
;(4)Na2O属于离子化合物,由钠离子与氧离子构成,用Na原子、O原子电子式表示氧化钠形成过程为:
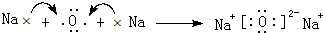 ,
,故答案为:
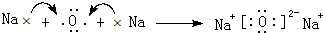 .
.
点评:本题考查原子结构与位置关系、电子式等,比较基础,注意掌握用电子式表示化学键或物质的形成过程.

练习册系列答案
相关题目
下列做法不能体现“环境友好”思想的是( )
| A、汽油抗爆:甲基叔丁基醚代替四乙基铅 |
| B、处理废弃物:对废弃塑料露天焚烧 |
| C、工业制胆矾:使用稀硫酸、双氧水溶解铜 |
| D、火力发电:在燃煤中加入适量生石灰 |
下列有关卤族元素的说法中不正确的是( )
| A、工业上以海水为原料,提取溴单质 |
| B、分别向新制氯水和久置的氯水中滴加AgNO3溶液都能生成白色沉淀 |
| C、可用干燥的有色布条检验氯化氢气体中是否混有Cl2 |
| D、医生建议患甲状腺肿大的病人多食海带,这是由于海带中含有较丰富的碘元素 |
某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO3-,现取两份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol?L-1的硫酸溶液恰好完全吸收,酸也不剩余.
根据上述实验,以下推测不正确的是( )
①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol?L-1的硫酸溶液恰好完全吸收,酸也不剩余.
根据上述实验,以下推测不正确的是( )
| A、原溶液一定不存在较大浓度的H+、Mg2+ |
| B、原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5:2:1 |
| C、不能确定原溶液是否含有K+、NO3- |
| D、实验中产生的棕色气体遇空气颜色会加深 |