题目内容
17.下列有关化学键与晶体结构说法正确的是( )| A. | 两种元素组成的分子中一定只有极性键 | |
| B. | 含有阴离子的化合物一定有阳离子 | |
| C. | 非金属元素组成的化合物一定是共价化合物 | |
| D. | 离子化合物的熔点一定比共价化合物的高 |
分析 A.H-O-O-H中含非极性键;
B.含有阴离子的化合物,一定为离子化合物;
C.非金属元素组成的化合物,可能为离子化合物;
D.一般来说,离子化合物的熔点比共价化合物的高.
解答 解:A.H-O-O-H中含非极性键,则两种元素组成的分子中可能含极性键、非极性键,故A错误;
B.含有阴离子的化合物,一定为离子化合物,则含阳离子,故B正确;
C.非金属元素组成的化合物,可能为离子化合物,如铵盐为离子化合物,故C错误;
D.一般来说,离子化合物的熔点比共价化合物的高,但二氧化硅的熔点比NaCl的高,故D错误;
故选B.
点评 本题考查离子化合物,为高频考点,把握化学键的形成及判断、常见物质中的化学键为解答的关键,侧重分析与应用能力的考查,注意结合实例分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.用下列装置能达到实验目的是( )
| A. |  分离酒精和乙酸 | B. |  制取少量蒸馏水 | ||
| C. |  转移溶液 | D. |  分离淀粉溶液中的水 |
8.下列化学用语书写正确的是( )
| A. | NH3分子的结构式: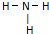 | B. | CO2分子模型的示意图: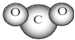 | ||
| C. | 氮分子的结构式:N=N | D. | HClO的电子式: |
5.下列物质的熔点,前者大于后者的是( )
| A. | 晶体硅、碳化硅 | B. | 甲苯、苯酚 | C. | 氧化镁、氧化钠 | D. | 钾钠合金、钠 |
2.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 垃圾是放错地方的资源,应分类回收利用 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 实现化石燃料清洁利用,就无需开发新能源 | |
| D. | 为提高农作物的产量和质量,应大量使用化肥和农药 |
9.下列有关实验操作及安全知识的叙述,正确的是( )
| A. | 实验室做钠的实验时,余下的钠屑投入到废液缸中 | |
| B. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 把玻璃管插入橡胶塞孔时,可用厚布护手,紧握用水湿润的玻管,缓慢旋进塞孔中 | |
| D. | 实验室制乙酸丁酯时,须用水浴加热 |
6.下列有机化学反应方程式及反应类型均正确的是( )
| 选项 | 化学反应方程式 | 反应类型 |
| A | CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3 | 酯化反应 |
| B | CH4+Cl2 $\stackrel{光照}{→}$CH3Cl+HCl | 置换反应 |
| C | CH2=CH2+Br2→CH3CHBr2 | 加成反应 |
| D | 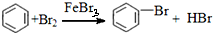 | 取代反应 |
| A. | A | B. | B | C. | C | D. | D |
7.下列说法正确的是( )
| A. | 化学键的形成一定伴随着电子的转移和能量变化 | |
| B. | NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同 | |
| C. | 24Mg32S晶体中电子总数与中子总数之比为1:1 | |
| D. | 某晶体固态不导电水溶液能导电,说明该晶体是离子晶体 |