题目内容
7.下列物质中所含的分子数相等的是( )①0.1mol CO2
②9.8g H2SO4
③1g H2O
④1.6g O2.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
分析 根据N=nNA可知,物质的量相等时含有的分子数相等,先分别计算出各物质的物质的量,根据计算结果进行判断.
解答 解:根据N=nNA可知,物质中所含的分子数相等,说明物质的物质的量相等,
①0.1mol CO2;
②9.8g H2SO4的物质的量为:$\frac{9.8g}{98g/mol}$=0.1mol;
③1g H2O的物质的量为:$\frac{1g}{18g/mol}$=$\frac{1}{18}$mol;
④1.6g O2的物质的量为:$\frac{1.6g}{32g/mol}$=0.05mol;
根据计算可知,物质的量相等的为①②,则含有分子数相等的为①②,
故选A.
点评 本题考查了物质的量的简单计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数之间的关系即可解答,试题侧重基础知识的考查,有利于提高学生的化学计算能力.

练习册系列答案
相关题目
18.下列各选项中所述的两个量,前者一定大于后者的是( ) )
| A. | 室温下,1L0.3mol•L-1CH3COOH溶液和3L0.1 mol•L-1CH3COOH溶液中的H+数 | |
| B. | 纯水在25℃和80℃时的pH | |
| C. | 在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数 | |
| D. | 相同条件下,H2分别与Cl2、F2反应的反应速率 |
12.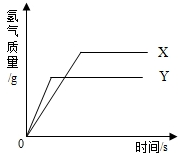 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中不正确的是( )
现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中不正确的是( )
 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中不正确的是( )
现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中不正确的是( )| A. | 生成氢气的质量:X>Y | B. | 相对原子质量:X>Y | ||
| C. | 金属活动性:Y>X | D. | 消耗硫酸的质量:X>Y |
19.下列物质属于化合物的是( )
| A. | 空气 | B. | 氧气 | C. | 食盐水 | D. | 二氧化锰 |
16.同温同压下,等体积的O2和CO2相比较,下列叙述正确的是( )
| A. | 质量比为11:8 | B. | 原子个数之比为2:3 | ||
| C. | 物质的量之比为3:2 | D. | 密度之比为8:11 |
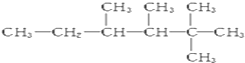 是某单炔烃与氢气加成后的产物,则此炔烃可能有1种结构,若该烷烃与氯气发生取代反应生成一氯代物有7种.
是某单炔烃与氢气加成后的产物,则此炔烃可能有1种结构,若该烷烃与氯气发生取代反应生成一氯代物有7种.