题目内容
可逆反应:4A(s)+3B(g)?2C(g)+D(g)(放热反应),2s末,B的浓度减小0.6mol/L,下列说法正确的是( )
| A、在2s时,A与B物质反应速率之比为4:3 | B、其他条件不变,升高温度,正反应速率减小,逆反应速率增大 | C、在2s时,D的物质的量一定增加0.2mol | D、若容器的温度和体积保持不变,反应前后容器的压强相等 |
分析:可以用不同物质表示化学反应速率,其反应速率之比为计量数(系数)之比,但是不一定要注意:能用纯固体或者纯液体表示化学反应速率;温度升高,化学反应速率一定增大;B浓度减小0.6mol/L,所以D浓度增加0.2mol/L,但是无法确定容器体积,所以不能确定物质的量的变化量;由于A物质为固体,观察反应方程式反应物和生成物气体计量数之和相等,所以反应前后气体的物质的量不发生变化,所以压强不变.
解答:解:A、由于A物质为固体,不能用来表示反应速率,故A错误;
B、升高温度,正逆反应速率都增大,故B错误;
C、2s时,D物质的量浓度一定增加0.2mol/L,但是不能确定物质的量的增加量,故C错误;
D、压强之比等于物质的量之比,反应前后气体的物质的量不变,所以反应前后容器压强相等,故D正确.
故选D.
B、升高温度,正逆反应速率都增大,故B错误;
C、2s时,D物质的量浓度一定增加0.2mol/L,但是不能确定物质的量的增加量,故C错误;
D、压强之比等于物质的量之比,反应前后气体的物质的量不变,所以反应前后容器压强相等,故D正确.
故选D.
点评:该题考查化学反应速率的相关知识,还考查了阿伏伽德罗定律的推论.学生必须准确掌握纯固体和纯液体能否表示化学反应速率以及影响化学反应速率的因素,同时注意选项中设置的一些陷阱.

练习册系列答案
相关题目
下列图示与对应的叙述相符的是( ) 
图1 图2 图3 图4
A.图1表示反应2NO(g)+2CO(g)  N2(g)+2CO2(g)平衡常数K 随NO物质的量的变化 N2(g)+2CO2(g)平衡常数K 随NO物质的量的变化 |
B.图2中表示反应2A(g) + B(g) 2C(g) ΔH > 0的平衡常数K随温度的变化 2C(g) ΔH > 0的平衡常数K随温度的变化 |
C.图3表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的大 3C(g)+D(s)的影响,乙的压强比甲的大 |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在5左右 |
下列图示与对应的叙述相符的是

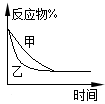

图1 图2 图3 图4
| A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图2表示0.1000 mol·L-1CH3COOH溶液滴定20.00mL0.1000 mol·L-1NaOH溶液所得到的滴定曲线 |
C.图3表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右 |
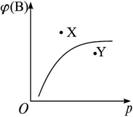

 N2O4已经达到平衡。
N2O4已经达到平衡。