题目内容
下列溶液中有关物质的量浓度关系正确的是( )
| A、0.1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| B、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) |
| C、物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=c(H+)+c(CH3COOH) |
| D、pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:A.0.1 mol/L的NaHA溶液,其pH=4,说明HA-的电离程度大于水解程度;
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液,强碱溶液浓度最小,弱酸根离子水解程度越大,其钠盐溶液浓度越小;
C.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液,强碱溶液浓度最小,弱酸根离子水解程度越大,其钠盐溶液浓度越小;
C.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
解答:
解:A.0.1 mol/L的NaHA溶液,其pH=4,说明HA-的电离程度大于水解程度,则c(H2A)<c(A2-),故A错误;
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液,强碱溶液浓度最小,弱酸根离子水解程度越大,其钠盐溶液浓度越小,水解程度CO32->CH3COO-,所以pH相等时,这三种溶液浓度大小顺序是c(NaOH)<c(Na2CO3)<c(CH3COONa),故B错误;
C.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒得c(CH3COO-)+c(OH-)=c(H+)+c(Na+),根据物料守恒得c(CH3COO-)+c(CH3COOH)=2c(Na+),所以得c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),故C错误;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒c(H+)+c(M+)=c(OH-)+c(A-),故D正确;
故选D.
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液,强碱溶液浓度最小,弱酸根离子水解程度越大,其钠盐溶液浓度越小,水解程度CO32->CH3COO-,所以pH相等时,这三种溶液浓度大小顺序是c(NaOH)<c(Na2CO3)<c(CH3COONa),故B错误;
C.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒得c(CH3COO-)+c(OH-)=c(H+)+c(Na+),根据物料守恒得c(CH3COO-)+c(CH3COOH)=2c(Na+),所以得c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),故C错误;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒c(H+)+c(M+)=c(OH-)+c(A-),故D正确;
故选D.
点评:本题考查了离子浓度大小比较,明确溶液中的溶质、溶液酸碱性再结合守恒思想分析解答即可,注意:任何电解质溶液中都存在电荷守恒和物料守恒,与电解质强弱、溶液酸碱性无关,为易错点.

练习册系列答案
相关题目
下列物质中不能导电的是( )
| A、稀硫酸 | B、钠 |
| C、NaCl晶体 | D、自来水 |
同温同压下,1molHe和1molCH4具有相同的( )
| A、原子数 | B、质子数 |
| C、质量 | D、体积 |
Na2HPO4溶液中存在着下列电离平衡:HPO42-?H++PO43-,要使溶液中[HPO42-]、[H+]、[PO43-]均减小可采用的方法是( )
| A、加盐酸 | B、加生石灰 |
| C、加热 | D、用水稀释 |
下列表达方式错误的是( )
| A、CO2分子的结构式:O=C=O | ||
B、S2-的结构示意图: | ||
C、中子数为10的氧原子符号:
| ||
D、NaBr的电子式 |
下列说法中,错误的是( )
| A、键长越长,化学键越牢固 |
| B、成键原子间原子轨道重叠越多,共价键越牢固 |
| C、对双原子分子来讲,键能越大,含有该键的分子越稳定 |
| D、原子间通过共用电子对所形成的化学键叫共价键 |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、含[Ag(NH3)2]+的溶液:K+、OH-、NH3?H2O、Cl- | ||||
B、使甲基橙试液变黄色的溶液:Na+、Cu2+、HCO-3、N
| ||||
C、与Al能够产生H2的溶液:Mg2+、K+、S
| ||||
| D、含Fe(OH)3胶体的溶液:Na+、Fe2+、I-、SCN- |
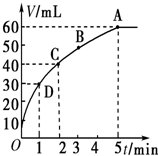 l mol MnO2粉末加入50mL过氧化氢的溶液里(ρ=1.1g?L-1),在标准状况下,放出气体的体积y和时间t的关系曲线如图所示.
l mol MnO2粉末加入50mL过氧化氢的溶液里(ρ=1.1g?L-1),在标准状况下,放出气体的体积y和时间t的关系曲线如图所示. 如图所示转化关系,已知A为气体单质,判断A是什么物质,并写出有关的化学方程式.
如图所示转化关系,已知A为气体单质,判断A是什么物质,并写出有关的化学方程式.