题目内容
可逆反应A(g)+3B(g)2C(g)△H=-QkJ/mol.有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1mol A和3mol B,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2mol C达到平衡后吸收热量为Q2 kJ;已知Q1=3Q2.下列叙述不正确的是( )
| A、甲中A的转化率为75% |
| B、Q1+Q2=Q |
| C、达到平衡后,再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向正向移动 |
| D、乙中的热化学方程式为2C(g) A(g)+3B(g)△H=+Q2kJ/mol |
考点:化学平衡的计算
专题:化学平衡专题
分析:由Q1=3Q2,可知△n甲(A)=3△n乙(A),设甲中达到平衡时转化了xmolA,则△n乙(A)=
mol,
甲 A(g)+3B(g)?2C(g)
起始(mol):1 3 0
转化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
乙 A(g)+3B(g)?2C(g)
起始(mol):0 0 2
转化(mol):
x x
x
平衡 (mol):
x x 2-
x
利用“一边倒法”,可知“1 mol A、3 mol B”与“2 mol C”是等效物料,它们在同温同容的条件下建立的平衡状态完全相同,则1-x=
,x=0.75,
α(A)=
×100%=75%,据此分析解答即可.
| x |
| 3 |
甲 A(g)+3B(g)?2C(g)
起始(mol):1 3 0
转化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
乙 A(g)+3B(g)?2C(g)
起始(mol):0 0 2
转化(mol):
| x |
| 3 |
| 2 |
| 3 |
平衡 (mol):
| x |
| 3 |
| 2 |
| 3 |
利用“一边倒法”,可知“1 mol A、3 mol B”与“2 mol C”是等效物料,它们在同温同容的条件下建立的平衡状态完全相同,则1-x=
| x |
| 3 |
α(A)=
| 0.75mol |
| 1mol |
解答:
解:由Q1=3Q2,可知△n甲(A)=3△n乙(A),设甲中达到平衡时转化了xmolA,则△n乙(A)=
mol,
甲 A(g)+3B(g)?2C(g)
起始(mol):1 3 0
转化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
乙 A(g)+3B(g)?2C(g)
起始(mol):0 0 2
转化(mol):
x x
x
平衡 (mol):
x x 2-
x
利用“一边倒法”,可知“1 mol A、3 mol B”与“2 mol C”是等效物料,它们在同温同容的条件下建立的平衡状态完全相同,则1-x=
,x=0.75,
α(A)=
×100%=75%,
A、甲中A的转化率为:α(A)=75%,故A正确;
B、若向相同容积的另一密闭容器中通入2molC,相当于1molA和3molB,达到平衡状态,从等效平衡的角度分析,则有Q=Q1+Q3,故B正确;
C、利用“一边倒法”,可知再加入“0.25 mol A、0.75 mol B、1.5 mol C”与再加入“2 mol C”等效,在恒温恒容条件下相当于增大压强,平衡向生成C的方向移动,故C正确;
D、乙中反应掉的C为
xmol=
=0.5mol,所给热化学方程式中2mol C对应的反应热应为:+4Q2 kJ?mol-1,故D错误;
故选D.
| x |
| 3 |
甲 A(g)+3B(g)?2C(g)
起始(mol):1 3 0
转化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
乙 A(g)+3B(g)?2C(g)
起始(mol):0 0 2
转化(mol):
| x |
| 3 |
| 2 |
| 3 |
平衡 (mol):
| x |
| 3 |
| 2 |
| 3 |
利用“一边倒法”,可知“1 mol A、3 mol B”与“2 mol C”是等效物料,它们在同温同容的条件下建立的平衡状态完全相同,则1-x=
| x |
| 3 |
α(A)=
| 0.75mol |
| 1mol |
A、甲中A的转化率为:α(A)=75%,故A正确;
B、若向相同容积的另一密闭容器中通入2molC,相当于1molA和3molB,达到平衡状态,从等效平衡的角度分析,则有Q=Q1+Q3,故B正确;
C、利用“一边倒法”,可知再加入“0.25 mol A、0.75 mol B、1.5 mol C”与再加入“2 mol C”等效,在恒温恒容条件下相当于增大压强,平衡向生成C的方向移动,故C正确;
D、乙中反应掉的C为
| 2 |
| 3 |
| 2×0.75mol |
| 3 |
故选D.
点评:本题考查了化学平衡的计算,题目难度较大,注意等效平衡的应用,解答该题时利用三段式法较为直观,试题综合性强,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
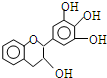

| A、分子中所有的碳原子共面 |
| B、1mol EGC与4molNaOH恰好完全反应 |
| C、易发生加成反应,难发生氧化反应和取代反应 |
| D、遇FeCl3溶液发生显色反应 |
在相同温度和相同浓度下的各种稀溶液中,下列各项排列可能不正确的是( )
| A、溶液的酸性:H2SO4>Al2(SO4)3>NH4NO3 |
| B、溶液的pH:Na2CO3>NaHCO3>CH3COONa |
| C、由水电离出的c(OH-):NaCl>HCl>NaOH |
| D、带电微粒数:Na2S>H2SO4>Mg(OH)2 |
现有如下5种无色溶液:NaAlO2、KOH、NaCl、MgCl2 稀氨水,若要将其一一鉴别开,至少需要用多少种试剂?( )
| A、不用试剂 | B、1种 |
| C、2种 | D、3种 |
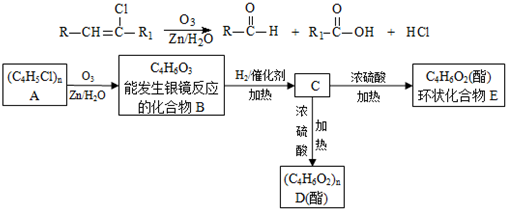
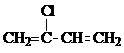 加聚而成,写出A的结构简式
加聚而成,写出A的结构简式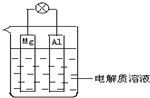 如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):