题目内容
用四种基本反应类型的分类方法,分析下列反应各属于哪种类型的反应.①2H2+O2
2H2O ②CuO+H2
Cu+H2O ③NH4HCO3
NH3↑+H2O↑+CO2↑④2CO+O2
2CO2 ⑤H2O+C
H2+CO ⑥Ba(OH)2+H2SO4═BaSO4↓+2H2O
(1)化合反应: .
(2)分解反应: .
(3)置换反应: .
(4)复分解反应: .
(5)氧化还原反应: .
| ||
| ||
| ||
| ||
| ||
(1)化合反应:
(2)分解反应:
(3)置换反应:
(4)复分解反应:
(5)氧化还原反应:
考点:化学基本反应类型,氧化还原反应
专题:
分析:置换反应:指一种单质和一种化合物生成另一种单质和另一种化合物的反应;
分解反应:指一种化合物分解成二种或二种以上较简单的单质或化合物的反应;
化合反应:指的是由两种或两种以上的物质生成一种新物质的反应;
复分解反应:是由两种化合物互相交换成分,生成另外两种化合物的反应;
氧化还原反应:有电子的得失或共用电子对的偏移的反应.
分解反应:指一种化合物分解成二种或二种以上较简单的单质或化合物的反应;
化合反应:指的是由两种或两种以上的物质生成一种新物质的反应;
复分解反应:是由两种化合物互相交换成分,生成另外两种化合物的反应;
氧化还原反应:有电子的得失或共用电子对的偏移的反应.
解答:
解:①2H2+O2
2H2O,反应物有2种,产物只有一种,故属于化合反应;氧的化合价由0价降低为-2价,故属于氧化还原反应;
②CuO+H2
Cu+H2O,反应物为一种单质和一种化合物,生成物为另一种单质和另一种化合物,故属于置换反应;铜的化合价由+2价降低为0价,故属于氧化还原反应;
③NH4HCO3
NH3↑+H2O↑+CO2↑,反应物只有一种,产物有3种,故属于分解反应;没有元素的化合价发生变化,故不属于氧化还原反应;
④2CO+O2
2CO2,反应物有2种,产物只有一种,故属于化合反应;氧的化合价由0价降低为-2价,故属于氧化还原反应;
⑤H2O+C
H2+CO,反应物为一种单质和一种化合物,生成物为另一种单质和另一种化合物,故属于置换反应;氢的化合价由+1价降低为0价,故属于氧化还原反应;
⑥Ba(OH)2+H2SO4═BaSO4↓+2H2O,反应物为两种化合物生成物为另外两种化合物,故属于复分解反应;没有元素的化合价发生变化,故不属于氧化还原反应;
故(1)属于化合反应的是:①④;(2)属于分解反应的是:③;(3)属于置换反应的是:②⑤;(4)属于复分解反应的是:⑥;(5)属于氧化还原反应的是:①②④⑤,
故答案为:(1)①④;(2)③;(3)②⑤;(4)⑥;(5)①②④⑤.
| ||
②CuO+H2
| ||
③NH4HCO3
| ||
④2CO+O2
| ||
⑤H2O+C
| ||
⑥Ba(OH)2+H2SO4═BaSO4↓+2H2O,反应物为两种化合物生成物为另外两种化合物,故属于复分解反应;没有元素的化合价发生变化,故不属于氧化还原反应;
故(1)属于化合反应的是:①④;(2)属于分解反应的是:③;(3)属于置换反应的是:②⑤;(4)属于复分解反应的是:⑥;(5)属于氧化还原反应的是:①②④⑤,
故答案为:(1)①④;(2)③;(3)②⑤;(4)⑥;(5)①②④⑤.
点评:本题考查了四种基本反应类型及氧化还原反应的判断,题目难度不大,注意要熟练掌握基本反应和氧化还原反应的特点.

练习册系列答案
相关题目
下列实验装置能达到相应实验目的是( )
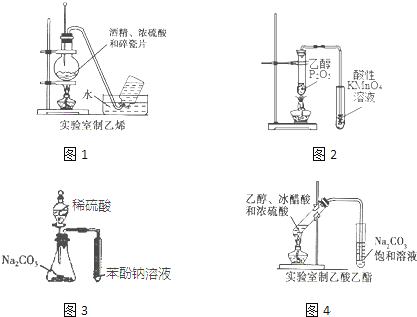

| A、图1装置一定可以制得乙烯 |
| B、图2装置可以证明CH3CH2OH发生消去反应生成了乙烯 |
| C、图3所示装置可以证明碳酸酸性强于苯酚 |
| D、实验室常用图4所示装置制取少量的乙酸乙酯 (夹持物略) |
胡椒酚是植物挥发油的成分之一,它的结构简式为:HO- -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )
 -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )| A、1mol胡椒酚最多可与4molH2发生反应 |
| B、1mol胡椒酚最多可与4mol溴发生反应 |
| C、胡椒酚中所有原子可以共平面 |
| D、胡椒酚在水中的溶解度小于苯酚在水中的溶解度 |
下列关于金属钠的叙述错误的是( )
| A、金属钠可以保存在煤油中 |
| B、金属钠着火时,可用泡沫灭火器来灭火 |
| C、钠与熔融的四氯化钛反应可制取钛 |
| D、实验时用剩的钠块应该放回原试剂瓶 |
设C+CO2═2CO(正反应吸热),该反应速率v1;N2+3H2?2NH3(正反应放热),该反应速率v2.若升温,v1和v2的变化是( )
| A、同时增大 |
| B、同时减少 |
| C、v1增大,v2减少 |
| D、v1减少,v2增大 |
某碱性蓄电池在充电和放电时发生的反应为:Fe+NiO2+2H2O
Fe(OH)2+Ni(OH)2,下列说法中正确的是( )
| 放电 |
| 充电 |
| A、放电时,负极上发生反应的物质是Fe |
| B、放电时,正极反应是:NiO2+2e-+2H+═Ni(OH)2 |
| C、充电时,阴极反应是:Ni(OH)2-2e-+2OH-═NiO2+2H2O |
| D、充电时,阳极应该是镍元素化合价降低 |
下列各组离子中,因相互促进水解,而不能大量共存的是( )
| A、Al3+、SO42-、CO32-、Cl- |
| B、Na+、HCO3-、AlO2-、Cl- |
| C、H+、HS-、Na+、SO32- |
| D、OH-、Na+、K+、HCO3- |
下列离子方程式正确的是( )
| A、碳酸钡与足量盐酸反应:2H++BaCO3=Ba2++H2O+CO2↑ |
| B、氯气通入蒸馏水中:Cl2+H2O=Cl-+ClO-+2H+ |
| C、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-+H++OH-=BaSO4↓+H2O |
| D、过量CO2通入澄清石灰水中:CO2+Ca(OH)2=CaCO3↓+H2O |