题目内容
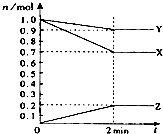 (1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:
(1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:(2)反应A(g)+3B(g)?2C(g)+2D(g),不同情况测得反应速率,其中反应速率最快的是
①υ(D)=0.4mol/(L?s)②υ(C)=0.5mol/(L?s)
③υ(B)=0.6mol/(L?s)④υ(A)=0.15mol/(L?s)
考点:化学平衡建立的过程,反应速率的定量表示方法
专题:化学平衡专题
分析:(1)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;根据v=
计算反应速率;
(2)反应速率的单位相同,用各物质表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
| △c |
| △t |
(2)反应速率的单位相同,用各物质表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
解答:
解:(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,
且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y 2Z;v(Z)=
2Z;v(Z)=
=0.05mol?(L?min)-1
故答案为:3X+Y 2Z;0.05mol?(L?min)-1
2Z;0.05mol?(L?min)-1
(2)反应速率的单位相同,用各物质表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快
①、
=0.2 mol/(L?s)
②、
=0.25mol/(L?s),
③、
=0.2mol/(L?s),
④、
=0.15mol/(L?s),
所以反应速率v(C)>v(B)v(D)>v(A).
故选:②.
且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y
 2Z;v(Z)=
2Z;v(Z)=| 0.2mol/2L |
| 2min |
故答案为:3X+Y
 2Z;0.05mol?(L?min)-1
2Z;0.05mol?(L?min)-1(2)反应速率的单位相同,用各物质表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快
①、
| υ(D) |
| 2 |
②、
| v(C) |
| 2 |
③、
| v(B) |
| 3 |
④、
| v(A) |
| 1 |
所以反应速率v(C)>v(B)v(D)>v(A).
故选:②.
点评:本题考查化学平衡图象分析题目,题目难度不大,注意分析各物质的量的变化曲线,把握化学方程式的判断方法;比较反应速率常用的两种方法:(1)归一法:将同一反应中的不同物质的反应速率转化成同一物质的反应速率,再较小比较.(2)比值法:用各物质的量表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
比较反应速率时注意(1)反应速率的单位要相同(2)单位时间内反应物或生成物的物质的量变化大,反应速率不一定快,反应速率是用单位时间内浓度的变化量来表示的
比较反应速率时注意(1)反应速率的单位要相同(2)单位时间内反应物或生成物的物质的量变化大,反应速率不一定快,反应速率是用单位时间内浓度的变化量来表示的

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
下列叙述中正确的是( )
| A、电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
| B、向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
| C、常温下,将pH=10的氨水稀释,溶液中所有离子浓度都减小 |
| D、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H>0 |
化学与人类生产、生活、社会可持续发展密切相关,下列说法不正确的是( )
| A、为防止富脂食品氧化变质,常在包装袋中放入生石灰 |
| B、“天宫一号”中使用的碳纤维,是一种新型无机非金属材料 |
| C、用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
| D、汽车排放的尾气和冬季取暖排放颗粒污染物是形成雾霾的重要因素 |
下列物质鉴别方法中,正确的是( )
| A、用淀粉溶液鉴别NaBr、KI溶液 |
| B、用KMnO4酸性溶液鉴别CH4、C2H4气体 |
| C、用AgNO3溶液鉴别Na2SO4、NaCl溶液 |
| D、用澄清石灰水鉴别Na2CO3、NaHCO3溶液 |
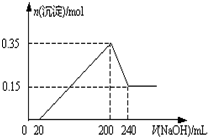 将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题:
将一定质量的Mg和Al的混合物投入2.0mol/L,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示.回答下列问题: