题目内容
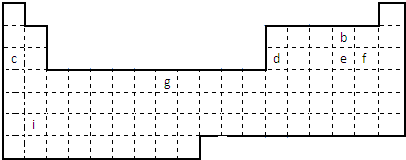
下表中所列的字母分别代表某一化学元素.
完成下列填空:
(1)b元素的原子有 种能量的电子.g元素的原子次外层电子数为 .
(2)d单质溶于i的最高价氧化物对应水化物的溶液时发生反应的离子方程式为 .
(3)元素e与f元素相比,下列表述中能证明非金属性较强的这一事实是 (选填序号).
a.e的阴离子还原性强于f的阴离子
b.f的氢化物稳定性性强于e的氢化物
c.e单质的熔点高于f单质
d.e和f形成的化合物中,e显正价,f显负价
完成下列填空:
(1)b元素的原子有
(2)d单质溶于i的最高价氧化物对应水化物的溶液时发生反应的离子方程式为
(3)元素e与f元素相比,下列表述中能证明非金属性较强的这一事实是
a.e的阴离子还原性强于f的阴离子
b.f的氢化物稳定性性强于e的氢化物
c.e单质的熔点高于f单质
d.e和f形成的化合物中,e显正价,f显负价

考点:位置结构性质的相互关系应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素的位置可知,c为Na,B为O,d为Al,e为S,f为Cl,g为Fe,i为Ba,
(1)O的质子数为8,有8种电子,Fe的电子排布为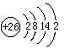 ;
;
(2)Al与Ba(OH)2反应生成Ba(AlO2)2和氢气;
(3)利用气态氢化物的稳定性、对应离子的还原性、化合物中元素的化合价比较非金属性,不能利用物理性质比较非金属性,以此来解答.
(1)O的质子数为8,有8种电子,Fe的电子排布为
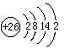 ;
;(2)Al与Ba(OH)2反应生成Ba(AlO2)2和氢气;
(3)利用气态氢化物的稳定性、对应离子的还原性、化合物中元素的化合价比较非金属性,不能利用物理性质比较非金属性,以此来解答.
解答:
解:由元素的位置可知,c为Na,B为O,d为Al,e为S,f为Cl,g为Fe,i为Ba,
(1)O的质子数为8,有8种电子,则有8种能量的电子;Fe的电子排布为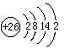 ,则原子次外层电子数为14,故答案为:8;14;
,则原子次外层电子数为14,故答案为:8;14;
(2)Al与Ba(OH)2反应生成Ba(AlO2)2和氢气,离子反应为2Al+2H2O+2OH-=2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;
(3)a.e的阴离子还原性强于f的阴离子,则e的非金属性强,故正确;
b.f的氢化物稳定性强于e的氢化物,则非金属性f的强,故正确;
c.e单质的熔点高于f单质,不能利用熔点比较非金属性,故错误;
d.e和f形成的化合物中,e显正价,f显负价,则f(Cl)的非金属性强,故正确;
故答案为:abd.
(1)O的质子数为8,有8种电子,则有8种能量的电子;Fe的电子排布为
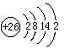 ,则原子次外层电子数为14,故答案为:8;14;
,则原子次外层电子数为14,故答案为:8;14;(2)Al与Ba(OH)2反应生成Ba(AlO2)2和氢气,离子反应为2Al+2H2O+2OH-=2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;
(3)a.e的阴离子还原性强于f的阴离子,则e的非金属性强,故正确;
b.f的氢化物稳定性强于e的氢化物,则非金属性f的强,故正确;
c.e单质的熔点高于f单质,不能利用熔点比较非金属性,故错误;
d.e和f形成的化合物中,e显正价,f显负价,则f(Cl)的非金属性强,故正确;
故答案为:abd.
点评:本题考查位置、结构与性质的关系及应用,为高频考点,把握元素的位置、性质及非金属性的比较为解答的关键,注意(2)与Al与NaOH反应相似,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
下列属于化石燃料的是( )
| A、氢气 | B、木柴 | C、煤 | D、酒精 |
欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的是( )
| A、乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液 |
| B、乙醇(水):加入新制生石灰,蒸馏 |
| C、溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 |
| D、乙酸(乙醇):加入金属钠,蒸馏 |
以下化石能源的加工所得产品不符合事实的是( )
| A、石油分馏-丙炔 |
| B、石油裂解-乙烯 |
| C、石油裂化-汽油 |
| D、天然气热分解-炭黑 |
MOH和ROH两种一元碱,其水溶液分别加水稀释时,pH变化如图所示.下列叙述中正确的是:( )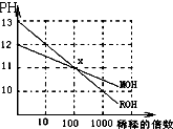

| A、在x点,ROH未完全电离 |
| B、在x点,c(M+)>c(R+) |
| C、稀释前,c(ROH)=10c(MOH) |
| D、pH=2的盐酸与pH=12的MOH等体积混合后,溶液显碱性 |
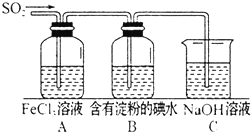 某兴趣小组探究SO2气体的性质,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体的性质,他们使用的药品和装置如图所示: