题目内容
13.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.表列出了①~⑨九种元素在周期表中的位置.| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ |
(1)这九种元素分别是①C(填元素符号,下同)、②O、③Na、④Mg、⑤Al、⑥Cl、⑦Ar、⑧K、⑨Br,其中化学性质最不活泼的是Ar.
(2)在③④⑤三种元素的最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式).其中③⑤元素的最高价氧化物对应的水化物发生反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O.
(3)①、②、③三种元素按原子半径由大到小的顺序依次为Na>C>O(填元素符号).
(4)⑧元素与⑥元素形成的化合物高温下灼烧时,火焰呈紫色.如何观察透过蓝色钴玻璃.
分析 (1)由元素在周期表中的位置可知,①是C、②是O、③是Na、④是Mg、⑤是Al、⑥是Cl、⑦是Ar、⑧是K、⑨是Br,其中稀有气体化学性质最不活泼;
(2)金属性越强,最高价氧化物对应水化物的碱性越强;氢氧化钠与氢氧化铝反应生成偏铝酸钠和水;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大;
(4)⑧元素与⑥元素形成的化合物KCl,钾元素的焰色反应为紫色.
解答 解:(1)由元素在周期表中的位置可知,①是C、②是O、③是Na、④是Mg、⑤是Al、⑥是Cl、⑦是Ar、⑧是K、⑨是Br,其中稀有气体Ar化学性质最不活泼,
故答案为:C;O; Na; Mg;Al;Cl;Ar; K; Br; Ar;
(2)非金属性Na>Mg>Al,金属性越强,最高价氧化物对应水化物的碱性越强,故NaOH的碱性最强;氢氧化钠与氢氧化铝反应生成偏铝酸钠和水,反应方程式为:Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:NaOH;Al(OH)3+NaOH=NaAlO2+2H2O;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>C>O,
故答案为:Na>C>O;
(4)⑧元素与⑥元素形成的化合物是KCl,钾元素的焰色反应为紫色,观察时需要透过透过蓝色钴玻璃,
故答案为:紫;透过蓝色钴玻璃.
点评 本题考查周期表和周期律的应用,为高频考点,侧重于分析与应用能力的考查,把握元素的位置和性质、元素周期律等为解答该题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.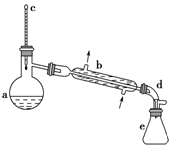 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
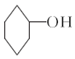 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$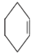 +H2O,
+H2O,
可能用到的有关数据如表:
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓H2SO4,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯12g.
回答下列问题:
(1)装置b的名称是直形冷凝管(或冷凝管).
(2)本实验中最容易产生的副产物的结构简式为 ,生成该物质的反应类型是取代反应
,生成该物质的反应类型是取代反应
(3)分液漏斗在使用前须清洗干净并检漏,在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)在环己烯粗产物蒸馏过程中,不可能用到的仪器有CE(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗D.锥形瓶 E.蒸发皿
(5)本实验所得到的环己烯产率是73.2%.
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图: $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O,
+H2O,可能用到的有关数据如表:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓H2SO4,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯12g.
回答下列问题:
(1)装置b的名称是直形冷凝管(或冷凝管).
(2)本实验中最容易产生的副产物的结构简式为
 ,生成该物质的反应类型是取代反应
,生成该物质的反应类型是取代反应(3)分液漏斗在使用前须清洗干净并检漏,在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)在环己烯粗产物蒸馏过程中,不可能用到的仪器有CE(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗D.锥形瓶 E.蒸发皿
(5)本实验所得到的环己烯产率是73.2%.
1.常温下,用pH=11的氨水,分别与pH=3的盐酸和某酸等体积混合,得到X、Y两种溶液,关于这两种溶液酸碱性的描述正确的是( )
| A. | X可能呈酸性 | B. | X溶液可能呈中性 | C. | Y溶液可能呈中性 | D. | Y溶液一定呈中性 |
8.部分弱酸的电离常数如表:
下列有关说法正确的是( )
| 弱酸 | HCOOH | HCN | H2S |
| 电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A. | 恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 | |
| B. | HCOO-、CN-、HS-在溶液中不可以大量共存 | |
| C. | NaHS溶液中加入适量KOH后:c(Na+)═c(H2S)+c(HS-)+2C(S2-) | |
| D. | 等体积、等浓度的HCOONa和NaCN两溶液中所含离子总数目HCOONa大于NaCN |
18.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 18 g D2O和18 g H2O中含有的质子数均为10 NA | |
| B. | 22.4 LC02中含有共价键数目4 NA | |
| C. | 若H2O2分解产生成0.1mol氧气转移的电子数为0.2 NA | |
| D. | 同温、同压同体积的CO和NO含有的电子数相等 |
5.下面有关晶体的叙述中,不正确的是( )
| A. | 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 | |
| B. | 12g石墨中含有σ键的个数为2NA (NA表示阿伏伽德罗常数) | |
| C. | 氯化铯晶体中,每个Cs+周围紧邻8个Cl- | |
| D. | 干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
2.烷烃的相对分子质量为72,跟氯气发生取代反应所得的一氯代物只1种,该烃是( )
| A. | CH3CH2CH2CH2CH3 | B. | 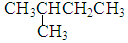 | ||
| C. | 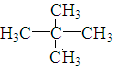 | D. | 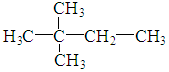 |