题目内容
(1)某化学反应,设反应物总能量为E1,生成物总能量为E2.若E1>E2,则该反应为 热反应,该反应的能量转化是 .
(2)中和反应都是 热反应,其实质是 .
(3)13g C2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,该反应的热化学方程式为 .
(2)中和反应都是
(3)13g C2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,该反应的热化学方程式为
考点:吸热反应和放热反应,热化学方程式
专题:
分析:(1)反应物总能量大于生成物总能量,为放热反应;
(2)中和反应为放热反应,酸和碱反应生成水;
(3)根据13gC2H2气体完全燃烧生成液态水和CO2,放出659kJ的热量,计算1molC2H2燃烧放出的热量,结合化学方程式书写热化学方程式.注意物质的聚集状态和反应热的单位等问题.
(2)中和反应为放热反应,酸和碱反应生成水;
(3)根据13gC2H2气体完全燃烧生成液态水和CO2,放出659kJ的热量,计算1molC2H2燃烧放出的热量,结合化学方程式书写热化学方程式.注意物质的聚集状态和反应热的单位等问题.
解答:
解:(1)设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为放热反应;能量转化是化学能转化为热能,故答案为:放;化学能转化为热能;
(2)中和反应都是放热反应,反应的实质为H++OH-═H2O,故答案为:放;H++OH-═H2O;
(3)C2H2气体完全燃烧反应的化学方程式为:2C2H2+5O2
4CO2+2H2O,13g C2H2气体n(C2H2)=
=0.5mol,放出659kJ的热量,则1molC2H2燃烧放出的热量为:659kJ×2=1318KJ,则热化学方程式为:C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1318KJ/mol,
故答案为:C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1318KJ/mol.
(2)中和反应都是放热反应,反应的实质为H++OH-═H2O,故答案为:放;H++OH-═H2O;
(3)C2H2气体完全燃烧反应的化学方程式为:2C2H2+5O2
| ||
| 13g |
| 26g/mol |
| 5 |
| 2 |
故答案为:C2H2(g)+
| 5 |
| 2 |
点评:本题考查能量变化和热化学方程式的书写,为高考高频考点,注意把握热化学方程式的书写方法,学习中注意相关基础的学习和体会,难度不大.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
为确定某溶液的离子组成,进行如下实验:根据实验以下推测正确的是( )
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
| A、一定存在SO32-离子 |
| B、一定存在CO32-离子 |
| C、一定存在Cl-离子 |
| D、可能存在HCO3-离子 |
将表面已经完全钝化的铝条,插入下列溶液中,不会发生反应的是( )
| A、稀硝酸 | B、硝酸铜 |
| C、稀盐酸 | D、氢氧化钠溶液 |
四种短周期元素的性质或结构信息如下表.下列推断错误的是( )
| 元素编号 | 元素性质或结构 |
| T | M层上有2对成对电子 |
| X | 元素最高正价是+7价 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | 单质是银白色固体、导电、密度比水小,与水剧烈反应、和氧气反应不同条件下产物不同 |
| A、T的氢化物是同族元素氢化物中沸点最低的 |
| B、X的最高价氧化物对应的水化物,是无机含氧酸中的最强酸 |
| C、离子半径从小到大的顺序:Y<Z<T<X |
| D、X、Y形成化合物的晶体类型与X、Z形成化合物的晶体类型不同 |
在一密闭容器中充入1mol H2和1mol I2,在一定条件下发生如下反应:H2(g)+I2(g)?2HI(g)
△H<0,下列描述正确的是( )
△H<0,下列描述正确的是( )
| A、保持容器体积不变,向其中充入1mol H2,反应速率加快 |
| B、保持压强不变,向其中充入N2,气体颜色不变 |
| C、保持体积不变,充入1 mol I2,平衡正向移动,气体颜色变浅 |
| D、升高温度,逆反应速率增大,正反应速率减小,平衡逆向移动 |
下列离子反应方程式和相对应的化学方程式正确的是( )
| A、Ca2++2OH-=Ca(OH)2↓ CaCO3+2NaOH=Ca(OH)2↓+Na2CO3 |
| B、Ba2++SO42-=BaSO4↓ Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C、Ag++Cl-=AgCl↓ AgNO3+NaCl=AgCl↓+NaNO3 |
| D、Fe3++3OH-=Fe(OH)3↓ FeCl3+3NH3?H2O=Fe(OH)3↓+3NH4Cl |
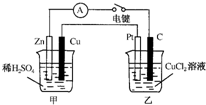 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题: 向某溶液A中逐滴加入或通入B物质至过量,反应过程中加入或通入B的量(用横坐标表示)与生成沉淀的量(用纵坐标表示)的关系如图所示,则符合图象的物质A与B为( )
向某溶液A中逐滴加入或通入B物质至过量,反应过程中加入或通入B的量(用横坐标表示)与生成沉淀的量(用纵坐标表示)的关系如图所示,则符合图象的物质A与B为( )