题目内容
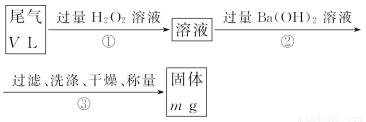
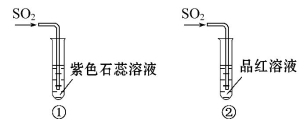
Na2O2、Cl2、SO2等均能使品红溶液褪色,下列说法正确的是 ( )
A.Na2O2、Cl2、SO2依次属于电解质、单质、非电解质
B.标准状况下,1 mol Na2O2和22.4 L SO2反应生成Na2SO4,转移电子数目为NA
C.等物质的量Cl2和SO2同时通入品红溶液,褪色更快
D.在Na2O2中阴阳离子所含的电子数目相等
A
【解析】
试题分析: Na2O2是离子化合物,属于电解质,Cl2由同种元素组成,属于单质,SO2属于非金属氧化物,自身不能电离出自由移动的离子,属于非电解质,故A正确;1 mol Na2O2和22.4 L SO2恰好反应生成Na2SO4,化学方程式为Na2O2+SO2====Na2SO4,反应中只有硫元素的化合价升高,由+4价升高为+6价,转移电子物质的量是SO2的2倍,转移电子物质的量为1 mol×2=2 mol,即2NA,故B错误;等物质的量Cl2和SO2同时通入品红溶液,发生反应Cl2+SO2+2H2O====2HCl+H2SO4,HCl、H2SO4没有漂白性质,故C错误;Na2O2中阴离子为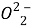 、阳离子为Na+,二者含有的电子数分别是18、10,故D错误。
、阳离子为Na+,二者含有的电子数分别是18、10,故D错误。
考点:二氧化硫的性质和作用

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 B
B D。
D。