题目内容
7.如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.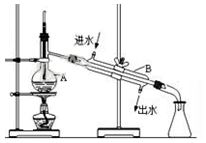
(1)指出图中明显的错误温度计插入蒸馏烧瓶中部的位置;冷凝管中水进入的方向;
(2)A仪器的名称是蒸馏烧瓶;B仪器的名称是冷凝管;
(3)分液的第一步操作是打开分液漏斗上端塞子.
分析 实验室制取蒸馏水,温度计的水银球在烧瓶支管口处,冷却水下进上出,由图可知仪器的名称,分液时先打开塞子,利用压强使液体流下,以此来解答.
解答 解:(1)图中明显的错误有温度计插入蒸馏烧瓶中部的位置、冷凝管中水进入的方向均错,故答案为:温度计插入蒸馏烧瓶中部的位置;冷凝管中水进入的方向;
(2)由图可知,A为蒸馏烧瓶,B为冷凝管,故答案为:蒸馏烧瓶;冷凝管;
(3)分液的第一步操作是打开分液漏斗上端塞子,使液体顺利流下,故答案为:打开分液漏斗上端塞子.
点评 本题考查混合物分离提纯,为高频考点,把握混合物分离提纯实验、实验操作为解答的关键,侧重分析与实验能力的考查,注意蒸馏、分液的应用,题目难度不大.

练习册系列答案
相关题目
3.有关X、Y、Z、W四种短周期元素性质的数据如表:
下列有关叙述中错误的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 66 | 70 | 143 | 160 |
| 主要化合价 | -2 | +5、+3、-3 | +3 | +2 |
| A. | X和Y能形成多种共价化合物 | |
| B. | 最简单氢化物的沸点:X>Y | |
| C. | 工业上常用电解Z的氯化物水溶液的方法制备Z单质 | |
| D. | Z和W的氧化物均能溶于Y的最高价氧化物对应的水化物溶液中 |
18.某些高温油炸食品含有丙烯酰胺.过量的丙烯酰胺可引起食品安全问题.关于丙烯酰胺叙述不正确的是( )
| A. | 能使酸性KMnO4溶液褪色 | B. | 能发生加聚反应 | ||
| C. | 能与乙醇发生酯化反应 | D. | 能与氢气发生加成反应 |
15.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和的FeCl3溶液中 |
| B | 区分碳酸钠和碳酸氢钠两种溶液 | 用氢氧化钡溶液分别滴加,观察现象 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | CCl4萃取碘水中的I2 | 先从分液漏斗下口放出有机层,后从上口倒出水层 |
| A. | A | B. | B | C. | C | D. | D |
2.下列实验操作中错误的是( )
| A. | 蒸发操作时,当有大量晶体析出时停止加热,用余热使水蒸发 | |
| B. | 蒸馏操作中冷凝管的冷却水应下进上出 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 浓硫酸的稀释可以在量筒中进行 |
19.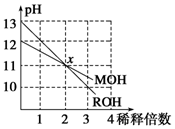 MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示.下列叙述中正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示.下列叙述中正确的是( )
 MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示.下列叙述中正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示.下列叙述中正确的是( )| A. | MOH和ROH都是强碱 | |
| B. | 稀释前,ROH=10MOH | |
| C. | 常温下pH之和为14的醋酸和ROH溶液等体积混合,所得溶液呈碱性 | |
| D. | 在x点,M+=R+ |
16.下列各项中表达正确的是( )
| A. | F原子结构示意图: | B. | 次氯酸电子式H Cl O | ||
| C. | H、D、T表示同一种核素 | D. | CO2的结构式为O═C═O |
17.某研究小组为探究饱和NaHCO3溶液中是否还能溶解少量NaHCO3固体,设计并完成了下列实验.
已知常温下:Ksp(CaCO3)=4.96×10-9,Ksp(MgCO3)=6.82×10-6
碳酸的电离常数:H2CO3?HCO3-+H+ K1=4.3×10-7
HCO3-?CO32-+H+ K2=5.6×10-12
Mg(OH)2沉淀范围:pH 9.4~12.4
(1)用化学用语解释饱和NaHCO3溶液pH为8.3的原因:HCO3-+H2O?H2CO3+OH-.
(2)实验③中若用CaCl2溶液代替MgCl2溶液完成实验,会观察到白色沉淀.现象不同的原因是溶液中存在平衡HCO3-?CO32-+H+,Ksp(CaCO3)<Ksp(MgCO3),说明Ca2+结合CO32-能力比Mg2+强,所以可以得到CaCO3沉淀.
(3)为探究NaHCO3固体溶解的原理,取实验④反应后的溶液,检验其产物.
Ⅰ.收集反应产生的气体,发现气体能使澄清的石灰水变浑浊.
Ⅱ.测得反应后烧杯中溶液的pH为8.7.
Ⅲ.向反应后的溶液中滴加MgCl2溶液,有白色沉淀生成.
①步骤Ⅲ中白色沉淀是MgCO3.
②结合化学用语解释饱和NaHCO3溶液中固体溶解的原因体系中存在平衡:2HCO3-(aq)?CO32-(aq)+CO2↑+H2O(l).由于CO2不断逸出,平衡正向移动,固体溶解.
③固体全部溶解后溶液pH升高的原因是反应生成了CO32-,由碳酸电离的常数可推出Na2CO3碱性大于NaHCO3,所以溶液pH升高.
(4)实验③的目的是验证检验饱和NaHCO3溶液中CO32-很少,不能与MgCl2溶液产生沉淀.
(5)根据上述实验得出的结论是饱和NaHCO3溶液中可以溶解少量的NaHCO3固体.
| 实验 编号 | 实验操作 | 现象或结论 |
| ① | 测饱和NaHCO3溶液的pH | pH为8.3 |
| ② | 向2mL Na2CO3溶液中加入MgCl2溶液 | 有白色沉淀生成 |
| ③ | 向2mL饱和NaHCO3溶液中加入MgCl2溶液 | 无明显现象 |
| ④ | 向20mL 饱和NaHCO3溶液中加入少量的NaHCO3固体,静置24小时 | 溶液中微小的气体缓慢地从底部固体逸出,最终固体全部溶解 |
碳酸的电离常数:H2CO3?HCO3-+H+ K1=4.3×10-7
HCO3-?CO32-+H+ K2=5.6×10-12
Mg(OH)2沉淀范围:pH 9.4~12.4
(1)用化学用语解释饱和NaHCO3溶液pH为8.3的原因:HCO3-+H2O?H2CO3+OH-.
(2)实验③中若用CaCl2溶液代替MgCl2溶液完成实验,会观察到白色沉淀.现象不同的原因是溶液中存在平衡HCO3-?CO32-+H+,Ksp(CaCO3)<Ksp(MgCO3),说明Ca2+结合CO32-能力比Mg2+强,所以可以得到CaCO3沉淀.
(3)为探究NaHCO3固体溶解的原理,取实验④反应后的溶液,检验其产物.
Ⅰ.收集反应产生的气体,发现气体能使澄清的石灰水变浑浊.
Ⅱ.测得反应后烧杯中溶液的pH为8.7.
Ⅲ.向反应后的溶液中滴加MgCl2溶液,有白色沉淀生成.
①步骤Ⅲ中白色沉淀是MgCO3.
②结合化学用语解释饱和NaHCO3溶液中固体溶解的原因体系中存在平衡:2HCO3-(aq)?CO32-(aq)+CO2↑+H2O(l).由于CO2不断逸出,平衡正向移动,固体溶解.
③固体全部溶解后溶液pH升高的原因是反应生成了CO32-,由碳酸电离的常数可推出Na2CO3碱性大于NaHCO3,所以溶液pH升高.
(4)实验③的目的是验证检验饱和NaHCO3溶液中CO32-很少,不能与MgCl2溶液产生沉淀.
(5)根据上述实验得出的结论是饱和NaHCO3溶液中可以溶解少量的NaHCO3固体.