题目内容
2.茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案测定某品牌茶叶中钙元素的质量分数,并检验铁元素的存在(已知CaC2O4为白色沉淀物质).首先取200g茶叶样品焙烧得灰粉后进行如图操作:
请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 4.1 |
(2)写出从滤液A→沉淀D的离子反应方程式Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试判断沉淀D已经洗涤干净的方法是取少量最后一次洗涤液于试管中,滴加碳酸钠溶液,若无白色沉淀则说明沉淀已洗涤干净.
(4)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+═10CO2↑+2Mn2++8H2O.
现将滤液C稀释至500mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.1000mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL.
①此步操作过程中需要用到图2中哪些仪器(填写序号)B、C、D;

②滴定到终点,静置后,如图3方法读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将偏高(填“偏高”“偏低”或“无影响”).
(5)原茶叶中钙元素的质量分数为0.3%.
(6)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及现象是加入KSCN溶液,溶液呈红色.
分析 测定某茶叶中钙元素的质量分数并检验铁元素的存在,取200g茶叶样品焙烧得灰粉,茶叶灰粉中加入3mol/L的足量硫酸溶液,过滤得到滤液A中主要是钙离子、铁离子等,加入氨水调节溶液PH=6,使铁离子全部生成氢氧化铁沉淀D,过滤得到滤液中加入草酸铵8.04g,过滤得到白色沉淀E为草酸钙,滤液C为硫酸铵溶液,
(1)将茶叶样品高温灼烧成灰粉,可以将有机物完全分解,将钙、铁等微量元素转化为可溶性物质,
(2)滤液A中含有铁离子,铁离子与氨水反应生成氢氧化铁沉淀,注意一水合氨为弱电解质,需要保留分子式;
(3)若氢氧化铁沉淀没有洗涤干净,氢氧化铁中会混有钙离子,可以使用碳酸钠溶液检验;
(4)①根据配制一定物质的量浓度的溶液方法及滴定操作方法选择使用的仪器;
②根据滴定结束前溶液为为无色,滴定结束时高锰酸钾溶液溶液过量进行解答;
③俯视液面导致滴定管中读数偏小,读出的高锰酸钾溶液体积偏小,计算出的钙离子消耗的草酸根离子物质的量偏大,测定结果偏高;
(5)根据滴定消耗高锰酸钾的物质的量计算出与钙离子反应剩余的草酸根离子的物质的量,再根据醋酸铵的总的质量及样品质量计算出钙离子的质量分数,注意滴定体积与样品体积的关系;
(6)根据检验铁离子遇到硫氰根离子溶液显示红色进行解答.
解答 解:(1)为了使检测更准确,需要将茶叶烧成灰粉,将样品中的有机物完全分解,将钙、铁等微量元素转化为可溶性物质,
故答案为:使样品中的有机物完全分解,将钙、铁等微量元素转化为可溶性物质;
(2)滤液中含有铁离子,铁离子与氨水反应生成红褐色的氢氧化铁沉淀,反应的离子方程式为:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,
故答案为:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+;
(3)检验氢氧化铁沉淀中是否洗涤干净,可以通过检验氢氧化铁中是否混有钙离子进行判断,方法为:取少量最后一次洗涤液于试管中,滴加碳酸钠溶液,若无白色沉淀则说明沉淀已洗涤干净,
故答案为:取少量最后一次洗涤液于试管中,滴加碳酸钠溶液,若无白色沉淀则说明沉淀已洗涤干净;
(4)①将滤液C稀释至500mL时需要使用到容量瓶,滴定操作中需要使用滴定管和锥形瓶,即B、C、D正确,
故答案为:B、C、D;
②滴定结束之前溶液为无色,滴定结束时高锰酸钾溶液过量,溶液变为紫色,所以滴定终点颜色变化为:无色变为紫色或高锰酸钾溶液不褪色,
故答案为:无色变为紫色或高锰酸钾溶液不褪色;
③滴定到终点,静置后,如图3读取KMnO4标准溶液的刻度数据,导致读数偏小,计算出的消耗的高锰酸钾溶液体积偏高,计算出的钙离子消耗的草酸根离子物质的量偏高,则测定的钙元素含量将偏高,
故答案为:偏高;
(5)8.04g草酸铵的物质的量为:$\frac{8.04g}{124g/mol}$=0.065mol,根据反应5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O可知与钙离子反应的草酸根离子的物质的量为:0.065mol-$\frac{5}{2}$×(0.10mol•L-1×0.01L)×$\frac{500ml}{25ml}$=0.015mol,根据化学式CaC2O4可知钙离子的物质的量为0.015mol,所以样品中钙离子的质量分数为:$\frac{40g/mol×0.015mol}{200g}$×100%=0.3%,
故答案为:0.3%;
(6)滤液A中含有铁离子,可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,方法为:取少量的滤液A,滴入硫氰化钾溶液,溶液变成红色,证明溶液中存在铁离子,也证明离子茶叶中含有铁元素,
故答案为:加入KSCN溶液,溶液呈红色.
点评 本题考查了探究茶叶中铁元素、钙元素的含量的方法及性质实验方案的设计,题目难度较大,注意掌握性质实验方案的设计方法,明确探究物质组成及含量的方法,试题培养了学生灵活应用所学知识解决实际问题的能力.

 阅读快车系列答案
阅读快车系列答案| 操作 | 现象 |
| 取适量漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝,后褪色 |
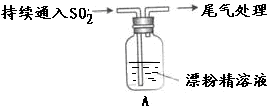 | 液面上方出现白雾; 稍后,出现浑浊,溶液变为黄绿色; 稍后,产生大量白色沉淀,黄绿色褪去 |
(2)向水中持续通入SO2,未观察到白雾.推测现象i的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a目的是验证Cl2是否存在;
②由实验a、b不能判断白雾中含有HC1,理由是与硝酸酸化的AgNO3产生的白色沉淀也可能是Ag2SO4或Ag2SO3;
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HC1,无明显变化.取上层清液,加入BaC12溶液,产生白色沉淀.则沉淀X中含有的物质是CaSO4
②用离子方程式解释现象iii中黄绿色褪去的原因:SO2+Cl2+2H2O=4H++SO42-+2Cl-.
(4)测定漂粉精有效成分的质量分数.称取2.000g漂粉精于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol•L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3C1O-+I-═3C1-+IO3-IO3-+5I-+3H2O═6OH-+3I2
实验测得数据如下表所示.
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
| A. | 向1 mol•L-1 AlCl3溶液中加过量的6 mol•L-1 NaOH溶液可制备Al(OH)3悬浊液 | |
| B. | 气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 | |
| C. | 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+ | |
| D. | 向含有少量Fe3+的CuSO4溶液中加入铜片可除去Fe3+ |
| A. | 有机化合物主要来自自然界众多的有机体 | |
| B. | 可以人工合成 | |
| C. | 有机物分子中的碳原子成键方式具有多样性 | |
| D. | 可以由无机物进行转化 |
| A. | O2 | B. | NH3 | C. | H2O | D. | CO2 |
| A. | A和B最简式一定相同 | B. | A和B不可能是同系物 | ||
| C. | A和B一定是同分异构体 | D. | A和B的化学性质相似 |
| A. | 2,2-二甲基-1-溴丙烷和2-甲基-2-溴丁烷 | |
| B. | 1,2-二甲苯和对二甲苯 | |
| C. | 2-甲基丁烷和戊烷 | |
| D. | 1-丁烯和1,3-丁二烯 |
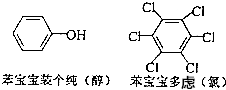 近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如右图所示).则苯酚的二氯代物同分异构体数目是( )
近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如右图所示).则苯酚的二氯代物同分异构体数目是( )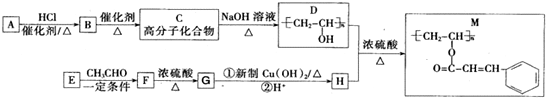

 .
.
 .
.