题目内容
20.下列除去CO2中的SO2杂质的方法中最佳的是( )| A. | 将气体通过澄清石灰水 | B. | 将气体通过氯水 | ||
| C. | 将气体通过KMnO4溶液 | D. | 将气体通过饱和KHCO3溶液 |
分析 二者均为酸性氧化物,而二氧化硫具有还原性,能被高锰酸钾、氯气氧化,但选项D中生成更多的二氧化碳,以此来解答.
解答 解:A.二者均与石灰水反应,不能除杂,故A不选;
B.二氧化硫与氯水反应,而二氧化碳不能,可除杂,但方法不最佳,故B不选;
C.二氧化硫与高锰酸钾反应,而二氧化碳不能,可除杂,但方法不最佳,故C不选;
D.二氧化硫与饱和KHCO3溶液反应生成二氧化碳,方法最佳,故D选;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
11.根据表中有关短周期元素性质的数据,判断下列说法中不正确的是( )
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| A. | ③和⑥、④和⑦分别处于同一主族 | |
| B. | 元素④处于第三周期ⅤA族 | |
| C. | 元素①与元素⑥形成的化合物中不可能存在共价键 | |
| D. | 元素⑧对应的氢氧化物可能具有两性 |
15.A、B、W、G、E代表五种短周期元素,有关他们的信息及性质如表所示.
(1)A元素在自然界中存在三种核素分别用符号H、D、T、表示,H2、D2、T2否(填‘是’或‘否’)互为同位素;
(2)B元素的最高价氧化物对应的水化物属于共价化合物(填‘离子化合物’或‘共价化合物’);
(3)W元素的最高价氧化物对应水化物能与其氢化物发生化合反应,反应方程式为HNO3+NH3=NH4NO3.
(4)元素G与元素E相比,非金属性较强的是氯(填元素名称),下列表述能证明这一事实的是b(填序号).
a.常温下E单质和G单质的密度不同;
b.E的氢化物比G的氢化物稳定;
c.E的氢化物水溶液酸性比G的氢化物水溶液酸性强
d.一定条件下G和E的单质都能与氢氧化钠溶液反应.
| 元素 | 元素性质或原子结构信息 |
| A | A元素的一种核素无中子 |
| B | B原子的次外层电子数等于最外层电子数的一半 |
| W | W的单质常温下为双原子分子,其氢化物的水溶液呈碱性 |
| G | G原子M层上有6个电子 |
| E | E元素的最高正价是+7 |
(2)B元素的最高价氧化物对应的水化物属于共价化合物(填‘离子化合物’或‘共价化合物’);
(3)W元素的最高价氧化物对应水化物能与其氢化物发生化合反应,反应方程式为HNO3+NH3=NH4NO3.
(4)元素G与元素E相比,非金属性较强的是氯(填元素名称),下列表述能证明这一事实的是b(填序号).
a.常温下E单质和G单质的密度不同;
b.E的氢化物比G的氢化物稳定;
c.E的氢化物水溶液酸性比G的氢化物水溶液酸性强
d.一定条件下G和E的单质都能与氢氧化钠溶液反应.
12.两元素可以形成AB2型离子化合物,它们的原子序数可能是( )
| A. | 12和8 | B. | 6和8 | C. | 20和9 | D. | 11和16 |
9.下列叙述中错误的是( )
| A. | H2在Cl2中燃烧、H2与Cl2的混合气体光照发生爆炸,都放出热量 | |
| B. | H2在O2中燃烧生成H2O放出能量,H2O分解为H2和O2吸收能量 | |
| C. | 氙和氟按一定比例混合,在一定条件下可直接发生反应:Xe+2F2═XeF4,该反应过程中Xe和F2都有化学键断裂 | |
| D. | 在CaO+H2O═Ca(OH)2的过程中CaO和H2O的总能量高于Ca(OH)2的总能量 |
 .
.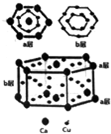 短周期元素A、B、C、D、E的原子序数依次增大,且原子最外层电子数之和为17.A是元素周期表中原子半径最小的元素,B原子的最外层电子数是其次最外层电子数的2倍,A与E同主族,D原子核外有2个未成对电子.
短周期元素A、B、C、D、E的原子序数依次增大,且原子最外层电子数之和为17.A是元素周期表中原子半径最小的元素,B原子的最外层电子数是其次最外层电子数的2倍,A与E同主族,D原子核外有2个未成对电子.