题目内容
8.下列叙述中错误的是( )| A. | 乙烯和苯使溴水褪色的原理不同 | |
| B. | 乙烯和聚乙烯中都有碳碳双键 | |
| C. | 煤的气化和液化都是化学变化 | |
| D. | 甲烷中混有乙烯时,仅用酸性KMnO4溶液不能提纯 |
分析 A.苯与溴水不反应;
B.聚乙烯中不含碳碳双键;
C.煤的气化生成CO和氢气,液化生成甲醇;
D.乙烯被高锰酸钾氧化生成二氧化碳.
解答 解:A.苯与溴水不反应,褪色为萃取原理,而乙烯与溴水发生加成反应,原理不同,故A正确;
B.聚乙烯中不含碳碳双键,乙烯含碳碳双键,故B错误;
C.煤的气化生成CO和氢气,液化生成甲醇,均有新物质生成,均为化学变化,故C正确;
D.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,则仅用酸性KMnO4溶液不能提纯,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
18.某原电池的总反应式是Zn+Cu2+═Zn2++Cu,该反应的原电池的正确组成是( )
| 选项 | A | B | C | D |
| 正极材料 | Zn | C | Zn | Mg |
| 负极材料 | Cu | Zn | Ag | Zn |
| 电解质溶液 | CuCl2 | CuSO4 | CuSO4 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
19.下列过程需要吸收热量的是( )
| A. | 甲烷在空气中燃烧 | B. | 碳酸钙受热分解 | ||
| C. | 镁条和盐酸反应 | D. | 氢氧化钠与盐酸反应 |
16.NA表示阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 1L0.1mol/L HCl溶液中含有0.1NA个HCl分子 | |
| B. | 23gNa在空气中燃烧生成Na2O2时转移电子数目为2NA | |
| C. | 28gCO和N2的混合气体中电子数目为14NA | |
| D. | 11.2LCO2含氧原子数为NA |
3.下列分子或离子中采用sp3杂化,但是V形结构的是( )
| A. | NH3 | B. | H2S | C. | BeCl2 | D. | NO3- |
13.天然气的主要成分是甲烷,液化气的主要成分是丁烷,欲将烧液化气的灶具改烧天然气,使燃料充分燃烧且灶具温度最高,下列操作正确的是( )
| A. | 减少进气量,增大进风量 | B. | 减少进气量,减少进风量 | ||
| C. | 不作任何改变 | D. | 增大进气量,减少进风量 |
17.下列判断不正确的是( )
| A. | 气态氢化物的热稳定性:H20>NH3 | |
| B. | 最高价氧化物对应水化物的酸性:H3PO4<H2SO4 | |
| C. | 原子半径:Na>Mg>Al | |
| D. | N元素的最高价氧化物对应的水化物和它的氢化物反应不能生成盐 |
18.下表为元素周期表的一部分,表中列出了10种元素在周期表中的位置,按要求完成下列各小题.
(1)化学性质最不活泼的元素的原子结构示意图为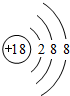 .
.
(2)元素⑧的名称为氯,其最高价氧化物的水化物的化学式为HClO4.
(3)元素③与元素⑧形成的化合物的电子式为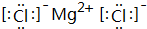 .
.
(4)非金属性最强的元素是F(填元素符号);除0族外原子半径最大的元素是K(填元素符号);元素①单质与水反应的离子方程式是2Na+2H2O=2Na++2OH-+H2↑.
(5)①、③、⑤三种元素的最高价氧化物为水化物中,碱性最强的化合物的化学式是NaOH.
(6)能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与①的最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ⑥ | ⑦ | ⑨ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | ||||
| 4 | ② | ④ |
 .
.(2)元素⑧的名称为氯,其最高价氧化物的水化物的化学式为HClO4.
(3)元素③与元素⑧形成的化合物的电子式为
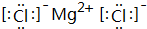 .
.(4)非金属性最强的元素是F(填元素符号);除0族外原子半径最大的元素是K(填元素符号);元素①单质与水反应的离子方程式是2Na+2H2O=2Na++2OH-+H2↑.
(5)①、③、⑤三种元素的最高价氧化物为水化物中,碱性最强的化合物的化学式是NaOH.
(6)能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与①的最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
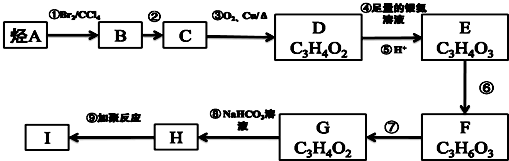
 .
. .
.