题目内容
5.下列化学用语表示不正确的是( )| A. | 钠离子的结构示意图: | |
| B. | 原子核内有20个中子的氯原子:${\;}_{17}^{37}$Cl | |
| C. | 氢氧根离子的电子式: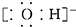 | |
| D. | NaHCO3的电离方程式:NaHCO3=Na++H++CO32- |
分析 A.钠离子的核电荷数为11,最外层达到8电子稳定结构;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
C.氢氧根离子为阴离子,电子式中需要标出所带电荷及最外层电子;
D.碳酸氢钠电离出钠离子和碳酸氢根离子,碳酸氢根离子不能拆开.
解答 解:A.钠离子的核电荷数为11,核外电子总数为10,其离子结构示意图为: ,故A正确;
,故A正确;
B.原子核内有20个中子的氯原子的质量数为37,该原子可以表示为:${\;}_{17}^{37}$Cl,故B正确;
C.氢氧根离子是带有1个单位负电荷的阴离子,其电子式为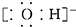 ,故C正确;
,故C正确;
D.NaHCO3为强电解质,在溶液中完全电离出钠离子和碳酸氢根离子,正确的电离方程式为:NaHCO3=Na++H++CO32-,故D错误;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及离子结构示意图、电子式、元素符号、电离方程式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及规范答题能力.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
15.以下数值大于或等于阿伏加德罗常数的是( )
| A. | 6g石墨中的共价键数目 | |
| B. | 常温常压下,17g ND3中所含分子数目 | |
| C. | 0.1mol羟基(-OH)中所含电子数目 | |
| D. | 向0.2mol NH4Al(SO4)2溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目 |
13.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) | |
| B. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+ )>c(OH-) | |
| C. | 20ml 0.1mol/L CH3COONa溶液与10ml HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)>c(OH-) | |
| D. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3- )>c(OH-) |
20.碳酸亚乙酯是一种重要的添加剂,其结构如图( ),碳酸亚乙酯可由两种分子发生酯化反应制取,这两种分子的原子个数比为( )
),碳酸亚乙酯可由两种分子发生酯化反应制取,这两种分子的原子个数比为( )
 ),碳酸亚乙酯可由两种分子发生酯化反应制取,这两种分子的原子个数比为( )
),碳酸亚乙酯可由两种分子发生酯化反应制取,这两种分子的原子个数比为( )| A. | 3:5 | B. | 1:2 | C. | 2:3 | D. | 2:5 |
10.某小组同学在实验室中研究+2和+3价铁的硝酸盐的化学性质.
(1)他们测硝酸亚铁溶液的pH常温下小于7,用离子方程式解释其原因是Fe2++2H2O?Fe(OH)2+2H+
(2)甲同学欲配制硝酸亚铁溶液,为防止水解,称量一定量硝酸亚铁晶体溶于pH=1的稀硝
酸中,溶液呈深棕色,液面上方有红棕色气体,放置一段时间,溶液最终呈黄色.
(已知:Fe2+能与NO结合形成深棕色的[Fe(NO)]2+:Fe2++NO?〔Fe(NO)]2+)
①液面上方红棕色气体是NO2
②经检验黄色溶液中有Fe3+.检验Fe3+的操作是取少量黄色溶液于试管中,滴入KSCN溶液,溶液显红色,证明含有Fe3+
③最初溶液中生成[Fe(NO)]2+使溶液呈深棕色,最终溶液变黄色的原因是在稀硝酸中Fe2+被NO3-氧化为Fe3+,使c(Fe2+)降低,Fe2++NO?〔Fe(NO)]2+的平衡向左移动,当Fe2+被完全氧化为Fe3+时,溶液由深棕色变为黄色
(3)甲同学继续用所得溶液进行实验.
①步骤i溶液中反应的离子方程式是2NO3-+3SO2+2H2O=3SO42-+2NO↑+4H+
②甲认为由步骤i的现象得出SO2与NO3-发生了反应,没有与Fe3+发生反应,请判断甲的结论是否正确并说明原因:正确.溶液上方产生红棕色的气体,说明NO3-被还原,溶液没有深棕色出现,说明Fe2+没有被氧化为Fe3+
③步骤ii溶液变为浅绿色,反应的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
④该实验得出的结论是SO2的还原性比Fe2+的强等
(1)他们测硝酸亚铁溶液的pH常温下小于7,用离子方程式解释其原因是Fe2++2H2O?Fe(OH)2+2H+
(2)甲同学欲配制硝酸亚铁溶液,为防止水解,称量一定量硝酸亚铁晶体溶于pH=1的稀硝
酸中,溶液呈深棕色,液面上方有红棕色气体,放置一段时间,溶液最终呈黄色.
(已知:Fe2+能与NO结合形成深棕色的[Fe(NO)]2+:Fe2++NO?〔Fe(NO)]2+)
①液面上方红棕色气体是NO2
②经检验黄色溶液中有Fe3+.检验Fe3+的操作是取少量黄色溶液于试管中,滴入KSCN溶液,溶液显红色,证明含有Fe3+
③最初溶液中生成[Fe(NO)]2+使溶液呈深棕色,最终溶液变黄色的原因是在稀硝酸中Fe2+被NO3-氧化为Fe3+,使c(Fe2+)降低,Fe2++NO?〔Fe(NO)]2+的平衡向左移动,当Fe2+被完全氧化为Fe3+时,溶液由深棕色变为黄色
(3)甲同学继续用所得溶液进行实验.
| 操作 | 步骤及现象 |
 | i:往溶液中缓慢通入SO2,液面上方有红棕色气体,溶液黄色无明显变化 ii:继续通入足量的SO2,溶液变为深棕色,一段时间后,溶液变为浅绿色 |
②甲认为由步骤i的现象得出SO2与NO3-发生了反应,没有与Fe3+发生反应,请判断甲的结论是否正确并说明原因:正确.溶液上方产生红棕色的气体,说明NO3-被还原,溶液没有深棕色出现,说明Fe2+没有被氧化为Fe3+
③步骤ii溶液变为浅绿色,反应的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
④该实验得出的结论是SO2的还原性比Fe2+的强等
14. 四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为N>O>C(用元素符号表示);试解释其原因同周期随原子序数增大第一电离能呈增大趋势,N元素2p轨道容纳3个电子,处于半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能由大到下的顺序为N>O>C.
(2)B元素的低价氧化物分子中心原子的杂化方式为sp2,B元素的最高价氧化物分子VSEPR模型为平面三角形,B元素与D元素形成分子空间构型为直线型.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是晶体类型不同,二氧化碳形成分子晶体,二氧化硅形成原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为先生成蓝色沉淀,后沉淀溶解生成深蓝色溶液;后一现象的化学反应方程式为Cu(OH)2+4NH3=[Cu(NH3)4](OH)2.
(5)某同学根据上述信息,推断A基态原子的核外电子排布为: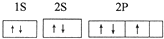
该同学所画的电子排布图违背了洪特规则.
(6)C晶体的堆积方式如图所示,设C原子半径为r cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{16}{\sqrt{2}{r}^{3}{N}_{A}}$g•cm-3(要求写表达式,可以不化简).
 四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.| 元素 | A | B | C | D |
| 性质 结构 信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx, 有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)B元素的低价氧化物分子中心原子的杂化方式为sp2,B元素的最高价氧化物分子VSEPR模型为平面三角形,B元素与D元素形成分子空间构型为直线型.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是晶体类型不同,二氧化碳形成分子晶体,二氧化硅形成原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为先生成蓝色沉淀,后沉淀溶解生成深蓝色溶液;后一现象的化学反应方程式为Cu(OH)2+4NH3=[Cu(NH3)4](OH)2.
(5)某同学根据上述信息,推断A基态原子的核外电子排布为:

该同学所画的电子排布图违背了洪特规则.
(6)C晶体的堆积方式如图所示,设C原子半径为r cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{16}{\sqrt{2}{r}^{3}{N}_{A}}$g•cm-3(要求写表达式,可以不化简).
15.氯气溶于水达到平衡后,若只改变某一条件,下列叙述正确的是( )
| A. | 通入少量SO2,溶液漂白性增强 | |
| B. | 加入少量NaHCO3固体,c(ClO)减小 | |
| C. | 加入少量水,水的电离平衡向正方向移动 | |
| D. | 加入NaOH固体至恰好完全反应,一定有c(Na+)=c(Cl-)+c(ClO-)+c(HClO) |



 .
. .
. .
.

 .
. .
. 等.(任写一种)
等.(任写一种)