题目内容
分别向1L 0.5mol/L NaOH溶液加入①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应的反应热分别为△H1、△H2、△H3,它们的关系正确的是( )
| A、△H1>△H2>△H3 |
| B、△H1>△H3>△H2 |
| C、△H1=△H2=△H3 |
| D、△H3>△H1>△H2 |
考点:反应热的大小比较
专题:
分析:25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ/mol,注意弱电解质的电离吸热,浓硫酸溶于水放热.
解答:
解:强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O△H=一57.3kJ/mol,分别向1L 0.5mol/L的NaOH溶液中加入:①稀醋酸;②浓H2SO4;③稀硝酸,醋酸的电离吸热,浓硫酸溶于水放热,则恰好完全反应时的放出的热量为②>③>①,所以△H2<△H3<△H1,故选B.
点评:本题主要考查了中和热大小的比较,需要注意的是弱电解质的电离吸热,浓硫酸溶于水放热以及比较大小时要考虑“-”号.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别是( )
| A、1000mL,212g |
| B、950mL,100.7g |
| C、任意规格,572g |
| D、500mL,286g |
在3S+6KOH═2K2S+K2SO3+3H2O的反应中,被还原的硫比被氧化的硫多3.2g,则参加反应硫的物质的量为( )
| A、0.1mol |
| B、0.2mol |
| C、0.3mol |
| D、0.4mol |
向0.1mol?L-1 CH3COOH溶液中加入CH3COONa晶体或加水稀释时,都会引起( )
| A、溶液的pH减小 |
| B、CH3COOH的电离程度增大 |
| C、溶液的导电能力减小 |
| D、溶液的c(OH-) 增大 |
下列事实或因果关系正确的是( )
| A、SO2的水溶液能导电说明SO2是电解质 |
| B、某溶液加NaOH溶液加热,产生气体使湿润红色石蕊试纸变蓝,则该溶液含有NH4+ |
| C、HClO是弱酸,所以NaClO是弱电解质 |
| D、某溶液中加入盐酸能产生使澄清石灰水变浑浊气体,则该溶液一定存在大量CO32- |
有关化学用语的表示正确的是( )
A、甲烷分子的比例模型是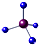 |
B、二氧化碳的电子式: |
C、Cl-的结构示意图为: |
| D、HClO的结构式为H-O-Cl |
对相同质量的SO2和SO3来说,下列关系正确的是( )
| A、含氧原子个数比为2:3 |
| B、含硫元素质量比为4:5 |
| C、含氧元素质量比为5:6 |
| D、含硫原子个数比为1:1 |
