题目内容
13. 如图所示,打开分液漏斗后,加热,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,则原烧杯中n(Na2S)与n(Na2SO3)的比值需满足( )
如图所示,打开分液漏斗后,加热,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,则原烧杯中n(Na2S)与n(Na2SO3)的比值需满足( )| A. | >2 | B. | <2 | C. | =2 | D. | 1~2之间 |
分析 通入HCl,发生Na2SO3+2Na2S+6HCl=3↓S+6NaCl+3H2O,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,说明硫化钠过量,以此解答该题.
解答 解:通入HCl,发生Na2SO3+2Na2S+6HCl=3↓S+6NaCl+3H2O,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,说明硫化钠过量,则 n(Na2S)>2n(Na2SO3),
故选A.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握反应的方程式的书写,难度不大.

练习册系列答案
相关题目
4.下列解释事实的反应方程式正确的是( )
| A. | 亚硫酸钠水溶液显碱性:SO32-+2H2O?H2SO3+2OH- | |
| B. | SO2的水溶液显酸性:SO2+H2O?H2SO3?2H++SO32- | |
| C. | 燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2 | |
| D. | 浓NaOH溶液处理少量二氧化硫:SO2+OH-═HSO3- |
8.下列物质与溴水混合振荡,溶液分层且上层有色、下层无色的是( )
| A. | 乙烯 | B. | 甲苯 | C. | 硝基苯 | D. | 甘油 |
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- | |
| B. | 0.1 mol/L的AlCl3溶液中:Na+、K+、SO42-、HCO3- | |
| C. | 25℃时,水电离出的c(H+)=1×l0-l3 mol/L的溶液中:K+、Ba2+、NO3-、S2- | |
| D. | 能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- |
9.下列叙述正确的是( )
| A. | 摩尔是一个物理量 | B. | 摩尔是粒子的数量单位 | ||
| C. | 4mol水分子中有8mol氢 | D. | 物质的量的单位是摩尔 |
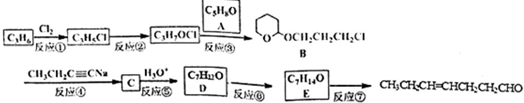
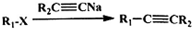
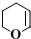 、CH3CH2C≡CCH2CH2CH2OH;
、CH3CH2C≡CCH2CH2CH2OH;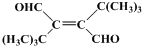 ;
;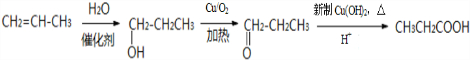 .
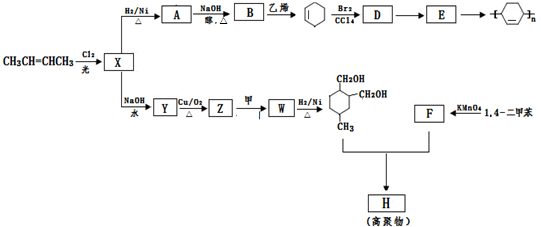
.
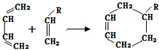 (或写成
(或写成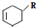 R代表取代基或氢)
R代表取代基或氢)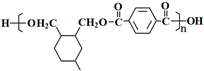 .
.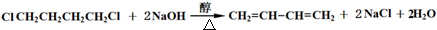 ;
;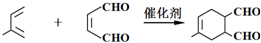 .
.
 ,属于弱电解质的是H2O、Al(OH)3.
,属于弱电解质的是H2O、Al(OH)3. 已知A、B、C、D、E、F六种化合物均由上述元素中的几种组成,它们之间的关系如图所示,A为淡黄色固体,B是常见液体,D是两性氧化物,F是引起酸雨的主要气体.
已知A、B、C、D、E、F六种化合物均由上述元素中的几种组成,它们之间的关系如图所示,A为淡黄色固体,B是常见液体,D是两性氧化物,F是引起酸雨的主要气体.